-
GC4419是一种高选择性、强效小分子歧化酶模拟物,可以模拟人类超氧化物歧化酶的活性,将超氧化物自由基分解为过氧化氢。由于超氧化物对正常细胞的损伤比癌细胞更大,而过氧化氢对癌细胞的毒性比正常细胞更大,歧化酶模拟物能够改变这一平衡,将超氧化物转化为过氧化氢,从而实现正常细胞和癌细胞对放射治疗的差异化效应。 -
GC4419需要在放射治疗前输注体内,可保护正常细胞并使癌细胞对放射治疗敏感。由于癌细胞比正常细胞更容易受到过氧化氢水平升高的影响,因此,利用歧化酶模拟物将多余的超氧化物转化为过氧化氢,有潜力提高放射治疗的抗癌效果。在多项临床前研究中已观察到,将歧化酶模拟物与高剂量放射治疗联合使用可提高抗癌疗效,这些证据支持了歧化酶模拟物联合放射疗法治疗实体瘤的生物学机制。
-
这项1/2期临床试验是一项随机、双盲、多中心、安慰剂对照试验,在42例确诊为LAPC的患者中开展,评估了SBRT与歧化酶模拟物GC4419方案、SBRT与安慰剂方案的安全性和有效性。研究中,患者随机(1:1)分别,在SBRT前一小时静脉输注GC4419或安慰剂。
-
GC4419治疗组的中位总生存期(OS)是安慰剂组的近2倍(中位OS:20.1个月 vs 10.9个月;HR=0.4)。 -
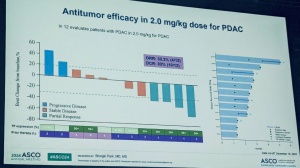
GC4419治疗组有29%患者病灶减少30%或更高的治疗缓解(部分缓解),而安慰剂组为11%(HR=0.4)。 -
在局部肿瘤控制(HR=0.3)、发生转移时间(13.9个月 vs 7.0个月)、无进展生存期(PFS;HR=0.4)方面也观察到阳性结果。 -
GC4419的耐受性良好,GC4419治疗组和安慰剂组的不良事件发生率相似。
-
胰腺癌是一种对放化疗敏感性差、切除率低的致死性恶性肿瘤。 -
该研究旨在观察白蛋白结合型紫杉醇+吉西他滨化疗+抗PD-1单抗联合同步放疗治疗潜在可切除的胰腺癌的疗效及不良反应。
-
LAPC或BRPC患者在第1天和第8天分别给予吉西他滨1000mg/m2和白蛋白紫杉醇125mg/m2,第1天给予替雷利珠单抗200mg Q3W。 -
两个周期治疗以后,同时进行SIB的低分割放射治疗(高剂量场:50 Gy/10次,剩余部分:30 Gy/10次)。4个疗程后再次评估手术可能性。 -
主要研究结果时ORR和R0切除率。次要终点包括安全性、mOS、mPFS,ctDNA。
-
从2020年5月到2021 10月,25名患者入选,中位年龄62岁。ORR为60%,DCR为100%。10例患者接受了切除,其中2例获得PCR,1例获得MPR。R0切除率为90%。 -
12个月OS率为79.4%,6个月PFS率为82.8%。 -
未观察到5级不良事件。2例(8%)均观察到3级或4级中性粒细胞减少和血小板减少。 -
非血液毒副作用包括黄疸(16%)、ALT/AST水平升高(20%)、呕吐(16%)、皮疹(12%)。
-
抗PD-1抑制剂加AG化疗,同时低分割放射治疗作为BRPC和LAPC患者的诱导治疗,具有显著的疗效和较好的安全性。
点击查看全文
本文仅供医学药学专业人士阅读




.jpg-pd13)



.png-pd13)
.jpg-pd13)












 X
X