胰腺癌,作为万癌之王,一直以来是令人闻风丧胆的存在。绝大多数胰腺癌患者发现的时候就已经是中晚期,绝大多数中晚期胰腺癌患者仅有的治疗手段就是化疗,接受化疗治疗的中晚期胰腺癌患者中位生存期不足1年。
在过去的20多年里,靶向治疗、免疫治疗等各种新型抗癌药物和抗癌技术,遍地开花,大幅度提高了绝大多数晚期实体瘤的疗效,显著地延长了绝大多数实体瘤患者的生存期。但是胰腺癌却是一个例外,截至目前:
PD-1抗体等免疫治疗对95%以上的胰腺癌患者无效;
唯一一个在胰腺癌中证实不俗疗效的靶向药是PARP抑制剂(奥拉帕利);但是奥拉帕利等PARP抑制剂,目前看来只对BRCA突变的胰腺癌患者有效,而BRCA突变在中晚期胰腺癌患者中阳性率只有5%-7%,言外之意超过90%的胰腺癌患者依然没有合适的分子靶向治疗药物可以用。
这种局面,近期被打破。85%-90%以上的胰腺癌患者都携带有KRAS突变,针对这部分患者,目前已经有各种各样的KRAS抑制剂,正在研发(详情请见:铁树开花:最难攻癌基因终于迎来神效靶向药)。
剩下的10%左右的KRAS突变阴性的胰腺癌患者,绝大多数携带NRG1突变,针对该突变,近期也迎来越来越多的靶向药。
首先,是广谱的HER家族抑制剂——阿法替尼。早在2019年,就有研究显示,阿法替尼治疗NRG1突变的实体瘤(肺癌、胰腺癌等等),具有不俗的疗效:
2例化疗失败的NRG1突变的晚期胰腺癌患者,接受了阿法替尼治疗,治疗后肿瘤均明显缩小、PET/CT提示肿瘤代谢降低、肿瘤标志物CA19-9明显下降、患者症状明显缓解;两例患者疗效分别维持5.5个月和超过5个月(截止作者发表论文时,治疗已满5个月,尚未出现疾病进展)。
上图是这两位患者治疗前后的PET/CT对比图:图A中治疗前肝脏弥漫的转移灶,治疗4周后几乎消退;图B中肝转移和多发的淋巴结转移,治疗4周后也明显缩小。

除了阿法替尼这个广谱的HER家族抑制剂,近日又有一款更高效、更低毒的双特异性抗体闪亮登场,这个药物名叫Zenocutuzumab。
所谓双特异性抗体,就像携带双弹头的高端弹道导弹,可以同时攻击两个靶子,只要癌细胞上表达任何一个靶子都会被命中且定点清除。Zenocutuzumab,是一个分别靶向HER2和HER3的双特异性抗体,研发出来主要是治疗NRG1突变的实体瘤,肺癌、乳腺癌、胰腺癌、肠癌、胃癌、肝癌等等,主要携带NRG1突变,均有机会起效。
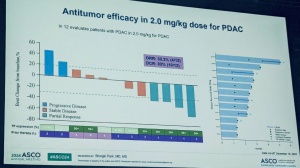
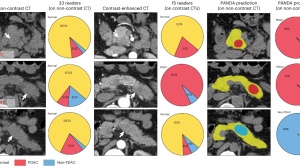
最初进入临床试验的3个病人,包括2个NRG1突变的化疗抵抗型胰腺癌和1个其他治疗失败(患者入组前接受过6种其他方案的治疗,均失败)的难治性肺癌患者。参加临床试验,接受了Zenocutuzumab治疗,两个胰腺癌患者肿瘤明显退缩,疗效维持时间均已超过1年,下图显示了其中1个患者治疗前后的CT和PET的变化:
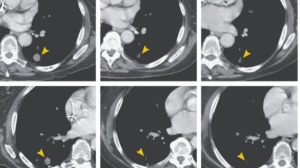
至于那个肺癌患者,入组前不仅接受过化疗、抗血管生成药物等6种不同方案药物的治疗,脑部接受过多次放疗,而且已经接受过阿法替尼靶向治疗、出现耐药,入组接受Zenocutuzumab治疗后,肿瘤同样显著缩小,患者症状明显改善。
上图展示了患者治疗后肿瘤体积随时间的变化以及治疗前后胸部CT的变化:可以明显发现,患者左肺的病灶大面积缩小。

基于这样亮眼的早期疗效,目前Zenocutuzumab正在全球各地开展针对NRG1突变的各类实体瘤的大规模临床试验,如果疗效数据可以继续保持,有望在不久的将来,正式上市。
[1]. NRG1 Gene Fusions Are Recurrent, Clinically Actionable Gene Rearrangements in KRAS Wild-Type Pancreatic Ductal Adenocarcinoma.Clin Cancer Res. 2019 Aug 1;25(15):4674-4681
[2]. Zenocutuzumab, a HER2xHER3 bispecific antibody, is effective therapy for tumors driven by NRG1 gene rearrangements. Cancer Discov. 2022 Feb 8;candisc.1119.2021. doi: 10.1158/2159-8290.CD-21-1119.
[3]. Maintenance Olaparib for Germline BRCA-Mutated Metastatic Pancreatic Cancer.N Engl J Med. 2019 Jul 25;381(4):317-327.












.png-pd13)
.jpg-pd13)












 X
X