中国的胃癌不仅多,而且由于筛查不足,多数发现就是晚期,生存率很差。尤其复发耐药后选择就非常少了作为是最常见的消化道肿瘤之一,胃癌已经严重威胁人类的生命健康。据世界卫生组织国际癌症研究机构(WHO IARC)发布的2020年最新全球癌症负担数据显示:2020年全球胃癌新发病例数达108.9万,位居第五;死亡病例数达76.8万,排在第四位;其中47.8万(43.9%)新发病例,其中有37.3万(48.5%)死亡病例就发生在中国!
ASCO-GI 2022圆满落幕
免疫数据新鲜出炉!
2022年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO-GI 2022)于近日以现场+虚拟会议形式召开,本届ASCO GI将讨论消化系统肿瘤领域最具创新性的科学进展。
1、首款胃癌双抗数据曝阳,卡度尼利单抗开启胃癌2.0时代
卡度尼利单抗(AK104)是一款PD-1/CTLA-4双特异性抗体药物。就在这场盛会上,其公布了用于联合化疗一线治疗胃/胃食管交界部癌Ⅰb/Ⅱ期临床研究数据。这项数据的披露,是胃癌治疗史上一个重要里程碑!
研究结果显示,截至2021年8月13日,入组的96例患者,44.8%具有肝转移。入组患者都要接受卡度尼利单抗(4、6、10mg/kg Q2W或10 、15mg/kg,Q3W)联合mXELOX化疗方案(mXELOX Q2W或XELOX Q3W)的治疗。
试验主要研究终点为ORR(RECIST v1.1)。
在中位随访时间为9.95个月中(0.4-26.8),有88例(92%)经过至少一次基线后肿瘤评估,ORR可达到65.9%(58-88),其中2(2.3%)例达到完全缓解(CR),56例(63.6%)达到部分缓解(PR);疾病控制率(DCR)为92.0%(81/88);中位持续缓解时间(DoR)为6.93个月(95% CI, 4.60-11.20);中位无进展生存(PFS)为7.10个月(95% CI,5.55-10.48);中位OS为17.41个月(95% CI, 12.35-NE)。
而在PD-L1 CPS≥1和CPS<1的患者中,中位OS分别为17.41个月和14.65个月。
治疗相关不良事件(TRAEs)发生率为97.9%,最常见的为血小板计数减少(60.4%),白细胞计数减少(58.3%),中性粒细胞计数减少(56.3%),贫血(47.9%),恶心(30.2%),呕吐(30.2%)和天冬氨酸转氨酶增加(30.2%)。3级及以上TRAE发生率为62.5%,没有新的安全性信号出现。
2、不受PD-L1表达水平限制,O药一线数据再次证明自己
2020年3月11日,中国胃癌患者迎来了首个获批用于晚期胃癌治疗的免疫肿瘤药物!是胃癌发展史上重要的程碑!2021年8月30日,欧狄沃经中国国家药品监督管理局(NMPA)批准欧狄沃(O药)联合含氟尿嘧啶和铂类药物化疗适用于一线治疗晚期或转移性胃癌、胃食管连接部癌或食管腺癌患者!
O药联合化疗方案不受PD-L1表达水平限制,在中国患者中,接受O药联合化疗方案的患者对比化疗可获得具有临床意义的总生存期(OS)与无进展生存期(PFS)双重获益,且取得了更高的客观缓解率(ORR)。
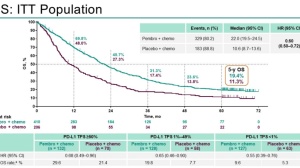
一项名为CheckMate -649的全球关键性III期临床研究在近日做出更新,旨在评估欧狄沃联合化疗,对比单独化疗用于晚期或转移性胃癌、胃食管连接部癌、食管腺癌一线治疗在全球(包括中国患者)人群中的疗效及安全性。
试验纳入2031例患者,其中有1581例随机分配至NIVO+化疗组或化疗组。在试验所有随机分组的患者中,NIVO+化疗组有41%患者、化疗组有44%的患者接受了后续治疗。NIVO+化疗组的中位PFS为12.2个月(95%CI 11.3-13.5),化疗组为10.4个月(95%CI 9.7-11.2)(HR 0.75 [95%CI 0.67-0.84])。
对于PD-L1 CPS≥10的患者,NIVO+化疗组的OS为15.0个月(95%CI 13.7-16.7),化疗组为10.9个月(95%CI 9.8-11.9)(HR 0.66 [95%CI 0.56-0.77])。与化疗组相比,NIVO+化疗组在多个亚组中观察到OS获益。未发现新的安全性信号。大多数具有潜在免疫学病因的治疗相关不良事件为1级或2级,在所有治疗组中,仅有不足5%的患者发生3级或4级不良事件。
K药胃癌一线数据再更新,
ORR可达74.4%!
小编观注到在《NATURE》发表了一篇关于帕博利珠单抗+曲妥珠单抗+化疗方案用于HER2阳性胃/胃食管连接癌一线治疗的3期临床研究。据悉,在2021年5月5日时,FDA就加速批准帕博利珠单抗(K药)+曲妥珠单抗+标准化疗用于胃癌一线治疗。
这是一项名为KEYNOTE-811随机、双盲、安慰剂对照Ⅲ期临床试验,旨在评估帕博利珠单抗或安慰剂联合曲妥珠单抗和化疗,作为进展期HER2阳性胃癌或胃食管交界处腺癌一线治疗的有效性和安全性。
研究共纳入 692 名患者,按 1:1 分配接受帕博利珠单抗 200 mg IV Q3W 或安慰剂 IV Q3W 长达 2 年或直至无法耐受毒性或 PD;所有参与者还接受标准剂量的曲妥珠单抗和研究人员选择的 5-氟尿嘧啶和顺铂(FP)或卡培他滨和奥沙利铂(CAPOX)。
主要终点为 OS 和 PFS,次要终点为 ORR 和 DOR。
在 264 例患者中进行的中期分析,帕博利珠单抗组的 ORR 为 74.4%[完全缓解(CR)率 11%,部分缓解(PR)率 63%],对照组组为 52%(CR 率 3.1%,PR 率 49%)(单侧 P 值 <0.0001)。接受帕博利珠单抗治疗的患者中位 DoR 为 10.6 个月,安慰剂组为 9.5 个月。
替雷利珠单抗,
胃癌一线OS显著改善
近日,百济神州的抗PD-1抗体替雷利珠单抗注射液联合化疗,一线治疗局部晚期、不可切除或转移性胃或胃食管结合部(G/GEJ)腺癌患者的全球性3期临床试验RATIONALE 305取得阳性结果。
试验共纳入997 名患者,均以1:1 的比例随机分配,分别接受:
(1)静脉注射 (IV) 替雷利珠单抗Q3W/200 mg+奥沙利铂和卡培他滨或替雷利珠单抗和顺铂/5-氟尿嘧啶 (5-FU);
(2)安慰剂和奥沙利铂/卡培他滨或安慰剂+顺铂/5-FU。
试验的主要终点是 OS。关键的次要终点包括无进展生存期 (PFS)、总缓解率 (ORR)、每个盲法独立审查委员会评估和 RECIST v1.1 标准的缓解持续时间 (DOR)、生活质量结果测量和安全性/耐受性。
结果显示,当用于肿瘤表达 PD-L1 的局部晚期、不可切除或转移性胃或胃食管结合部腺癌患者的一线治疗时,与单独化疗相比,替雷利珠单抗联合化疗显着提高了总生存期,符合 3 期 RATIONALE 305 的主要终点审判
信迪利单抗一线数据双阳
2021年11 月 4 日,NMPA受理了信达制药的信迪利单抗新适应症,联合化疗(奥沙利铂+卡培他滨)一线治疗不可切除的局部晚期、复发性或转移性胃或胃食管交界处腺癌。
在2021 ESMO 会议上 3 期 ORIENT-16 研究的数据也有了更新,ORIENT-16 研究是一项比较信迪利单抗或安慰剂,联合化疗(奥沙利铂+卡培他滨)一线治疗不可切除的局部晚期、复发性或转移性胃及胃食管交界处腺癌的有效性和安全性的随机、双盲、多中心、III 期研究(ClinicalTrials.gov, NCT03745170)。
主要研究终点为总体人群和 PD-L1 阳性人群的总生存期(OS)。
中位总生存期(mOS)在 CPS≥5 人群延长 5.5 个月(mOS 18.4 月 vs. 12.9 月),总体人群延长 2.9 个月(mOS 15.2 月 vs. 12.3 月)。总生存期在预设的所有亚组分析中获益趋势一致。安全性特征与既往报道的信迪利单抗相关临床研究结果一致,无新的安全性信号。
卡瑞利珠单抗联合化疗后序贯
卡瑞利珠单抗联合阿帕替尼,DCR 93.8%!
研究共纳入48例既往未接受全身治疗的HER2阴性的晚期或转移性G/GEJ腺癌患者。这些患者在接受卡瑞利珠单抗联合CAPOX化疗4-6周期后,序贯卡瑞利珠单抗联合阿帕替尼治疗。结果显示,OS为14.9个月,中位PFS为6.8个月,ORR为58.3%,DCR达93.8%。研究结果证实了该方案良好的抗肿瘤效果。
特瑞普利单抗联合化疗
一线ORR达66.7%!
这是一项开放标签、多中心、Ib/II期试验(NCT02915432),晚期胃癌患者被分为2个队列。在队列1中,58例化疗难治性晚期胃癌患者接受特瑞普利单抗单药治疗。在队列2中,18例化疗初治晚期胃癌患者接受特瑞普利单抗联合XELOX方案作为一线治疗。结果显示,队列2患者的ORR为66.7%,DCR为88.9%,中位PFS为5.8个月,中位OS未达到。
舒格利单抗联合化疗
一线治疗晚期胃癌,有效率62.1%!
基石药业宣布,其PD-L1抗体舒格利单抗(CS1001)联合化疗一线治疗GC/ GEJ和ESCC正在沈琳教授和李进教授的带领下开展国内多中心临床III期试验。2020 ESMO 2020大会上,报道了CS1001联合化疗一线治疗晚期胃癌患者的 Ib临床结果。有18(62.1%)例患者达到了部分缓解(PR),包括17例确诊的PR和1例未确诊的PR;6例(20.7%)患者疾病稳定(SD);3例(10.3%)患者发生疾病进展(PD)。中位缓解持续时间(mDoR)为11.3 个月,中位无进展生存期(mPFS)8.3个月,中位总生存期(mOS)17.0个月。
本文仅供医学药学专业人士阅读





.jpg-pd13)


.jpg-pd13)












 X
X