放疗在局部晚期食管癌治疗中发挥重要的作用,其临床价值并不逊于占主导地位的食管外科治疗。对于可手术食管癌,新辅助同步放化疗是术前标准治疗方案;对于不可手术食管癌,根治性放化疗是唯一的根治性方案[1]。
2015年首次发布结果的CROSS研究和2018年由中国学者牵头开展的NEOCRTEC 5010研究确立了同步放化疗在局部晚期可手术食管癌中的标准治疗地位[2,3]。与欧美国家食管癌以腺癌为主不同,我国食管癌95%以上为食管鳞状细胞癌(ESCC),对放射线相对敏感[4],但是由于各种原因,国内同步放化疗的临床实践并非主流,往往被放化疗序贯或单纯化疗取而代之。
2021年9月,程序性细胞死亡蛋白-1(PD-1)免疫检查点抑制剂帕博利珠单抗(商品名“可瑞达”,国内俗称“K药”)在国内获批联合铂类和氟尿嘧啶类化疗药物一线治疗局部晚期不可切除或转移性食管或胃食管结合部癌,推动我国晚期食管癌一线治疗迈入免疫时代。
已在晚期肺癌治疗中取得成功,且很快将正式“进军”晚期食管癌和胃癌的免疫+化疗治疗的“大火”,是否会“乘机”烧向食管癌新辅助治疗,从而撼动尚未“站稳脚跟”的放疗?食管癌放疗应该如何应对“来势凶猛”的免疫治疗,能否找到与免疫治疗共存的可能?是否能像III期不可切除非小细胞肺癌领域著名研究—PACIFIC研究所示,同步放化疗和免疫治疗各取所需,并协同增效?
金秋10月,帕博利珠单抗食管癌一线治疗适应证上市会召开。本平台特邀中国科学技术大学附属第一医院(安徽省立医院)肿瘤放疗科张红雁教授就KEYNOTE-590研究对食管癌临床实践影响,免疫治疗在食管癌围手术期治疗和不可切除局部进展期食管癌治疗中的潜力,以及给放疗带来的机遇分享个人观点。
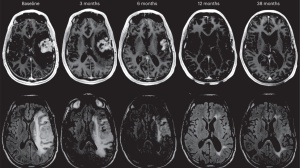
张红雁教授:食管癌是全世界最常见的恶性肿瘤之一,其死亡率也比较高。在过去几十年中,不管是手术、放疗还是化疗治疗食管癌,都遇到了瓶颈。作为放疗科医生,我看到放疗从二维时代进入三维时代,从普通放疗进入精准放疗,技术上得到了很大的提升,但是食管癌患者的生存状况并没有得到革命性的改变。
从KEYNOTE-181研究到KEYNOTE-590研究,帕博利珠单抗联合化疗治疗晚期食管癌从二线推进到了一线。KEYNOTYE-590研究的7个主要研究假设终点均得到了阳性结果,无论是在ITT人群,还是ESCC,或PD-L1 CPS≥10的ITT和ESCC人群中,K药联合化疗一线治疗在总生存期(OS),无进展生存期(PFS),客观缓解率(ORR)和缓解持续时间(DOR)数据上显示了相比单纯化疗一线治疗显著的优越性,安全性数据则与标准化疗相当[5]。
A:PD-L1 CPS≥10的ESCC人群;B:ESCC人群;C;PD-L1 CPS≥10的人群;D:ITT人群
帕博利珠单抗联合化疗获批食管癌一线治疗适应证并得到国内指南推荐,给患者带来福音的同时,也给临床医生在毒副反应管理和疗效精准预测等方面带来了挑战,未来还需要开展更多的研究来指导临床实践。
张红雁教授:手术是早期和局部进展期食管癌的重要治疗手段,但是手术只是解决了当时肉眼可见病灶,还会残留一些肉眼看不到的亚临床病灶。即使外科医生有再好的手术条件、经验和技巧,也难以完全彻底切除肿瘤。对于有高复发风险的pT2患者,pT3和pT4a患者或淋巴结阳性的患者,美国国家综合癌症网络(NCCN)指南推荐术后辅助治疗。对于R0切除后无淋巴结转移的pTis和pT1患者,目前指南没有推荐术后辅助治疗,但是临床上可以看到不少无淋巴结转移的pT1患者在术后出现复发和转移。
由于食管癌术后进食情况改变,患者营养和身体状况往往很差,很多患者术后瘦了十几斤,对标准辅助放化疗的耐受性通常不是特别好。在KEYNOTE-181研究中,帕博利珠单抗单药组3-5级治疗相关不良事件的发生率为18.2%,而化疗组为 40.9%[6]。基于免疫治疗在局部晚期和转移性食管癌治疗中展现出的良好疗效和安全性,目前研究者比较看好免疫治疗在食管癌辅助治疗中的潜力,认为术后免疫维持治疗可以充分调动自身免疫功能,攻击亚临床肿瘤,让肿瘤细胞没有力量再“造反”,从而降低复发风险。
张红雁教授:帕博利珠单抗联合放疗或化疗用于食管癌新辅助治疗是当前的研究热点。不同专业的医生思考角度不同,化疗医生可能提出免疫联合化疗,不做放疗;外科医生可能认为化疗“杀敌一千自损八百”,而放疗虽然对局部控制好,术后切缘阴性的患者更多,但是切缘水肿是否影响围手术期安全和术后愈合,因此会提出去掉化疗和放疗,仅使用免疫新辅助治疗;作为放疗科医生,我们会考虑免疫联合放疗,目前我们正在开展免疫治疗联合放疗用于食管癌新辅助治疗的研究。
放疗在食管癌中的应用有着悠久历史,但是接受放疗治疗的患者总体五年生存率仍然徘徊在15%-30%之间,存在复发转移问题。免疫治疗带来了一个新武器,为食管癌放疗带来诸多发展机遇。对于没有手术机会的患者,同步放化疗后可以使用免疫治疗维持治疗。
根据我们的经验,广泛纵隔淋巴结转移的患者在放疗后加上免疫治疗维持,目前已经取得了近三年的OS。放疗可以刺激免疫功能,相当于一个火箭助推器,能够让患者走得更远。希望未来免疫联合放疗在食管癌治疗中可以取得好的结果,我本人对这种治疗模式充满希望,相信曙光就在前方。
[1]中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)食管癌诊疗指南[M]. 北京:人民卫生出版社,2021.
[2]Joel Shapiro, J Jan B van Lanschot, Maarten C C M Hulshof, et al. Neoadjuvant chemoradiotherapy plus surgery versus surgery alone for oesophageal or junctional cancer (CROSS): long-term results of a randomised controlled trial[J]. Lancet Oncol
[3]Hong Yang, Hui Liu, Yuping Chen, et al. Neoadjuvant Chemoradiotherapy Followed by Surgery Versus Surgery Alone for Locally Advanced Squamous Cell Carcinoma of the Esophagus (NEOCRTEC5010): A Phase III Multicenter, Randomized, Open-Label Clinical Trial[J]. J Clin Oncol. 2018 ;36(27):2796-2803.
[4]中华人民共和国国家卫生健康委员会. 原发性肺癌诊疗规范(2018年版)[EB/OL].[ 2018-12-21].
[5]Jong-Mu Sun, Lin Shen, Manish A Shah, et al. Pembrolizumab plus chemotherapy versus chemotherapy alone for first-line treatment of advanced oesophageal cancer (KEYNOTE-590): a randomised, placebo-controlled, phase 3 study[J].Lancet. 2021;398(10302):759-771.
[6]Takashi Kojima, Manish A Shah, Kei Muro, et al. Randomized Phase III KEYNOTE-181 Study of Pembrolizumab Versus Chemotherapy in Advanced Esophageal Cancer J Clin Oncol[J].2020;38(35):4138-4148.







.jpg-pd13)
.jpg-pd13)















 X
X