珍女士是一个企业的老总。经过几年的打拼,事业渐入佳境。
但是,如果人生是一场宴席,总会有不速之客闯入。
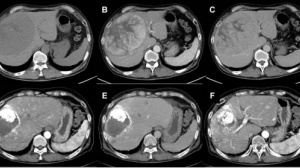
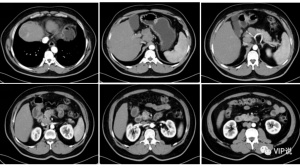
2015年10月,珍女士尚未到40。她注意到自己肚脐附近有一个肿块,到医院进行了腹部/骨盆CT检查,发现在双侧子宫有囊性占位性病变,医生倾向于认为是恶性卵巢肿瘤。同时,在右侧肝包膜下有结节。
三个星期后,医院给珍女士做了一个大手术,这个大手术包括许多个手术:探查性剖腹手术、肿瘤细胞减少术、全腹子宫切除术、双侧输卵管卵巢切除术、大网膜切除术、肝肿块切除术、横隔隔膜肿瘤切除术,横隔隔膜修复术、盆腔淋巴结切除、脐带杂音切除、直肠修复术、膀胱修复术和粘连溶解术。
做这么多的手术,都是迫不得已。在探查性剖腹手术之后,发现问题很大,癌细胞侵染的组织太多,包括输卵管、宫颈、子宫、直肠、乙状结肠、骨盆底、肝脏表面等等。不但要把侵染的癌组织切下来,还要对受到损伤的组织进行修复。
对手术切下的组织进行的病理检查,确诊了珍女士所患的是高级别浆液性卵巢癌,左侧肿瘤长度为3.0厘米,右侧肿瘤5.0厘米。癌细胞除了侵入上述的一些组织,还有淋巴管浸润,骨盆淋巴结也有转移,虽然转移灶很小,不到1毫米。
珍女士的病理期诊断为IIIC(3C),癌细胞还只是在肝脏表面。如果侵入了肝脏,那就是IV期了(4期)。
对于IIIC期的卵巢癌,因为情况已经比较严重,在手术之后都要进行化疗,一般是6个周期。
在手术之后,珍女士也老老实实开始了化疗,治疗方案是卡铂联合紫杉醇。前 4个周期在国内医院进行。2016年2月,珍女士到了美国A医院,继续完成了第5、6周期的化疗。
到美国之后,珍女士进行了基因突变检查,发现携带有BRCA1基因突变。
时间到了2016年年底,珍女士的病情此时还没有明显的复发,但是盆腔影像学检查看到了肿块。
2017年3月,珍女士的CA125指标升高到206。CA125是一个重要卵巢癌血液标志物,正常值为0~35单位/毫升,常常用于监测卵巢癌是否复发。如果CA-125升高,又在影像学检查中看到变大的肿块,可以判定为病情复发。
4月初,珍女士因为有BRCA1基因突变,参加了一个PARP抑制剂奥拉帕利的临床试验。在这个临床试验中,患者接受奥拉帕利联合 mTORC1/2 抑制剂AZD2014或 AKT抑制剂AZD5363的治疗。
这个临床试验让珍女士坚持了近一年。到了2018年2月,检查发现珍女士的病情发生了进展,于是结束了临床试验的治疗,改为进行多柔比星联合卡铂化疗。
2018年6月,腹部/骨盆CT检查显示,阴道穹处有肿瘤,被乙状结肠包绕,引起大肠梗阻;双侧肾积水,远端输尿管肿瘤浸润;上腹部肿瘤稳定。在检查之后,珍女士再次进行手术。跟两年半前的大手术相比,这次比较简单,只做了探索性剖腹手术、粘连溶解术、横向结肠造口术。
2018年8月, CT 显示晚期癌变进展,无肠梗阻。胸部没有看到转移性疾病。之后的一个月,珍女士短暂地参与了ATR抑制剂BAY1895344的一个开放标签的II期临床试验。
2018年9月,珍女士再次进行化疗,方案为紫杉醇联合贝伐单抗,共6个周期,至2019年3月结束。
2019年3月的CT检查显示,左锁骨上淋巴结自2018年12月无改变;腹股沟和肠系膜出现新的淋巴结肿大,骨盆淋巴结变大,腹膜后淋巴结稳定;腹膜癌变稳定。
2019年4月,珍女士参加了一项Wee1 抑制剂AZD1775的临床试验。
2019年5月,继续化疗,方案为拓扑替康和贝伐单抗。6月,化疗因为牙痛暂停。
2019年6月,乳腺钼靶检查发现左乳出现可疑的异常病灶,随后的活检证实为卵巢恶性肿瘤转移病灶。
2019年7月,珍女士双下肢水肿,延伸至下腹壁。CA125指标从6月初的1747继续飙升至4157。继续托泊替康和贝伐单抗化疗。
2019年8月,出现肝转移,腹膜癌灶变大,出现中度腹水。骶前、梨状肌和臀肌出现浸润性软组织转移病灶,中线腹壁也有转移病灶,有新的骨转移。胸腔积液也有所增加。
鉴于目前的治疗已经无法控制CA125的迅速上升,病灶也已经转移到乳房,所在的医院没有更好的办法,珍女士积极寻找第二医疗建议,求助于美国纽约纪念斯隆凯特琳癌症中心的卵巢癌外科主任Dr. Dennis Chi。
在视频电话问诊会议上,珍女士提出的是她最关心的问题:有没有办法改善生活质量?
珍女士说目前最大的折磨是肛门周围疼痛,而且由于骨盆腔中的肿瘤所产生的挤压,导致静脉回流严重受到影响,导致下肢水肿。
在仔细参看了CT扫描结果之后,Dr.Chi看到珍女士盆腔内的大肿块所累及的是乙状结肠和膀胱,但是骨盆侧壁和外血管都没有病变;上腹部似乎有癌变,但是并不广泛。但是,CT扫描是在2019年5月做的,不知道目前是否有进展?同时,CT报告里对会阴及肛门周围的分辨率也不是很清楚。
通常对于这样晚期的患者,是不会进行手术的,因为手术出现并发症的可能性很大,而且进行过手术的区域,还是会有癌症复发。但是,万事都有例外,根据珍女士的CT扫描结果,Dr. Chi认为确实可以进行姑息手术,切除目前在盆腔内的肿块,以减轻疼痛和不适。
如果珍女士的生活质量确实受到了严重的影响,需要考虑接受手术,Dr. Chi也要亲自先对珍女士进行检查,在确认病情的进展之后,才能进行手术。
在与Dr. Chi会诊之后,珍女士决定到纽约纪念斯隆凯特琳癌症中心进行手术,因为肛门周围的疼痛确实太难受了。
Dr. Chi再次对珍女士的现状进行了检查。很不幸,与上次CT检查的结果相比,珍女士盆腔底的肿瘤进展了,骨盆之间都没有了空间。如果要强行进行手术,患者恢复会非常困难。
此时,因为珍女士身体状况很差,医生认为不适合长途飞行。珍女士无法飞越太平洋,回到国内。
既然无法回去,就只有想想其他的治疗办法。几经周折,珍女士又找到美国加州大学欧文分校医学院的教授Dr. Nader Javadi进行会诊。
鉴于珍女士无法进行姑息手术,Dr. Javadi认为只有通过系统治疗,也许能对珍女士的病情有所缓解。Dr. Javadi提供的治疗建议是化疗+PD1免疫治疗+PARP抑制剂+贝伐单抗。
除了PD1免疫治疗,珍女士之前都单用或者部分联合使用过这几个药物,但是从来没有同时一起治疗过。之前在M医院,因为珍女士有乙肝病毒感染,医生没有给她使用PD1免疫治疗,因为担心会因此激活乙肝病毒,导致肝损伤。
Dr. Javadi认为,在经过多轮化疗后,珍女士的乙肝感染稳定,不一定会因PD1免疫治疗而激活,也许值得最后一试。
不想错失最后一个治疗的机会,珍女士决定到Dr.Javadi所在的医院进行治疗。
因为血红蛋白太低,珍女士连短途飞行都有问题。按照医生的建议,珍女士在进行输血之后,血红蛋白提高到8以上,才从M医院出院,随即飞到Dr. Javadi的医院所在地。
珍女士接受的治疗,是培美曲塞+PD1抗体O药+白蛋白紫杉醇+贝伐单抗注射治疗,外加奥拉帕利口服。
本来CA125的指标已经是6000多,但是在治疗之后,竟然降到了200多!
骨盆里的肿瘤也有好转,连下肢的水肿都有所好转。有几天,珍女士在搀扶之下,甚至可以在医院里走动走动。
珍女士抗癌的路,如今已经走了4年。这一路非常不容易。
孩子还小,虽然珍女士很想陪伴孩子高考,送孩子上大学,看到孩子结婚生子,但是她知道自己无法坚持到那一天。
珍女士的坚持,是因为身后有一个公司。她知道自己一倒,公司就垮了。当初创业,给一起创业的小伙伴们画了一张饼。珍女士不想让这张饼消失。
这里记录珍女士四年的抗癌路程,并不是因为它是一个范本。珍女士的道路是一条艰难的道路,如果珍女士对此有什么总结,应该是:希望谁都不要走上这条道路。
根据美国的统计,卵巢癌是美国女性中第五大最常见的癌症死亡原因, 也是妇科癌症的主要死亡原因,每年约有14000例死亡 [1]。
卵巢癌之所以比较恶性,是因为大约60%的患者在检查出病情时已经比较晚期,癌细胞已经出现了扩散。对于没有症状的健康人,目前缺乏一种可靠的卵巢癌筛查手段,将癌症发现于早期。CA125虽然是一个卵巢癌血液标志物,但是由于有比较高的假阳性,不适合用于对健康人进行筛查。研究发现,使用CA125进行筛查,不但不能有效降低卵巢癌死亡率,还会让不少女性进行不必要的手术。因此,美国预防医学工作组并不建议对健康人进行卵巢癌筛查[1]。
复盘一下治疗过程,如果能够从头再来一次,珍女士可能会选择什么道路呢?
虽然一般人没有必要进行卵巢癌筛查,但是珍女士并不属于一般人。她有BRCA1突变。
BRCA1突变是一个家族遗传突变,类似的还有BRCA2基因突变。携带这些遗传突变的家族,会出现更多的癌症患者。
如果一个家庭里有人发现携带这些突变,美国预防医学工作组建议所有有血缘关系的亲属都应该进行基因检查,确认是否自己也遗传了相关突变。为了预防癌症,携带BRCA的个体不但需要进行比较频繁的癌症检查,甚至可能需要采取比较激进的预防措施。
美国好莱坞影星安吉丽娜就有这个家族性遗传突变。她娘家出现了不少癌症患者,包括因卵巢癌去世的妈妈和因乳腺癌去世的小姨,以及得前列腺癌的舅舅、得汗腺癌的外公。为了预防乳腺癌,安吉丽娜在2013年作了双侧乳腺切除。两年后,她又手术切除了卵巢和输卵管,以预防卵巢癌。
人不可能让时间的河流逆转,珍女士无法回到许多年前,在生完孩子后就进行某些预防性手术。但是,其他有BRCA突变的人,需要知道有安吉丽娜的选项。
人也不可能两次踏入同一条河。珍女士于2015年检查出癌症,虽然奥拉帕利于2014年已经在美国获得批准,用于治疗有BRCA突变的卵巢癌,但是这个药在2018年才正式在中国获得批准。在2017年,珍女士参加了一个奥拉帕利的临床试验,总算没有错过使用这个PARP抑制药物的机会。
在2018年,奥拉帕利在美国进一步获得批准,作为一线维持治疗,用于有BRCA突变的卵巢癌患者。如果珍女士是在2018年检查出癌症,那在手术和首次化疗之后,医生将会马上给她使用奥拉帕利作为维持治疗,以延缓病情的复发,获得更好的治疗效果。
而另外一个PARP抑制药物尼拉帕利,在最近的临床试验中也显示出了很好的结果。不管卵巢癌患者是否有BRCA突变,尼拉帕利都能作为一线化疗后的维持治疗,把患者的中位无进展生存从8.2个月提高到13.8个月!如果是同源重组缺陷型患者(包括BRCA突变者),中位无进展生存可以达到21.9个月[2]。
当然,尼拉帕利这个一线维持治疗的结果刚出来,目前正式获得批准的适应症还是二线辅助治疗,但是,目前的标准临床治疗方案预期将很快会改变,将尼拉帕利辅助治疗也推到一线,让即便没有BRCA突变的患者,也多一个治疗的选择。
从2016年开始,珍女士在美国的治疗,一直是在M医院。这是美国一家非常好的肿瘤医院。在这里,珍女士也有机会接受一些新的临床试验。
但是,在治疗的问题上,从来没有从一而终这回事,即便是世界上最好的医院。这是为什么才有“第二诊疗意见”这样的选项。
如果珍女士不是等到今年夏天才通过爱医传递找到其他医院的医生咨询第二诊疗意见,她就有机会接受姑息性手术,早早把盆腔里的瘤子摘除;或者,她就有机会在身体还没那么糟糕的时候,开始“化疗+PD1免疫治疗+PARP抑制剂+贝伐单抗”这样的治疗,及时控制住病情的进展。
时间的河流不会停止,没有人可能穿越回去重新做出选择。但也因为时间的河流没有停止,医学一直在进步,对于珍女士这样的患者来说,治疗的选项会越来越多。
对于其他的“珍女士”,希望她们能走上一条更有希望的道路。
当然,对于晚期患者来说,这条道路可能是金钱铺成的道路,如果家里有矿,这条路可以铺得更长一点。
但这条路,也不是只要有钱就能铺成,也不是说这条路铺到了美国,肯定就比别人长。
抗癌的医疗技术在进步,治疗的选项越来越多。在美国,也可以及时寻找“第二诊疗意见”,可以让这路更长。

1. US Preventive Services Task Force, Screening for Ovarian Cancer: US Preventive Services Task Force Recommendation Statement. JAMA, 2018. 319(6): p. 588-594.
2. González-Martín, A., et al., Niraparib in Patients with Newly Diagnosed Advanced Ovarian Cancer. New England Journal of Medicine, 2019.
(作者:张洪涛,笔名“一节生姜”。宾夕法尼亚大学医学院病理及实验医药系研究副教授,研究领域:癌症的靶向治疗以及免疫治疗。著有科普读物:《吃什么呢?——舌尖上的思考》,《如果舌尖能思考》。可以谈最前沿的医学研究,也可以讲最通俗的故事。本文纯属科普,为保护隐私,患者名使用了化名。若有具体病情,请找靠谱的医生诊断。题图:Johannes Plenio from Pixabay)










.jpg-pd13)













 X
X