肝癌患者有新药了!
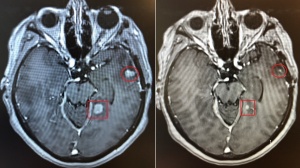
日前,制药公司Can-Fite BioPharma宣布[1],旗下在研肝癌药物Namodenoson在罗马尼亚获批作为同情用药治疗晚期肝癌患者,已有一位接受治疗的患者完全缓解,全身的转移灶全都消失。目前,相关III期研究已经开始进行,正在招募患者。
而且,不同于以往肝癌药物的研究主要在肝功能较好、Child-Pugh评分为A级(5~6分)的患者中进行,Namodenoson的研究还纳入了肝功能已经处于临界状态的B级(7~9分)患者,可以让更多的肝癌患者获益。
在所有癌症中,肝癌算是比较难治的一种。因为肝癌的发展往往要经历肝炎-肝硬化-肝癌三部曲,大多数肝癌患者同时还伴有肝硬化等其它肝脏的问题,肝功能较差。而包括抗癌药在内的很多药物都有一定的肝毒性,可能会进一步损害患者的肝功能,抗癌的益处会被肝功能的恶化所抵消[2]。
正因如此,很多肝癌药物都只能用于肝功能较好、Child-Pugh评分为A级的患者,而对肝功能处于临界状态的B级患者和处于失代偿状态的C级患者效果不佳。
比如说目前肝癌一线治疗的头牌索拉非尼,治疗Child-Pugh评分为A级的患者,中位生存期能有13个月,而B级患者只有4.5个月[3]。
而Namodenoson的作用机制十分特殊,它是一种A3腺苷受体(A3AR)的激动剂。在肿瘤组织中,Namodenoson可以增加促凋亡蛋白和FasL的表达,诱导癌细胞凋亡,而在正常组织中,Namodenoson却能抑制炎症,减轻缺血再灌注损伤,保护正常的肝细胞[4]。
癌细胞和炎性细胞表面高表达A3AR,而正常细胞几乎不表达
在此前的II期临床试验中[5],共有78名Child-Pugh评分为B级的晚期肝细胞癌患者接受了Namodenoson或安慰剂的治疗。由于全部9名Child-Pugh评分为9的患者都被意外分到了Namodenoson组,两组患者的中位总生存期分别为4.1个月和4.3个月,没有显著差距。
不过在Child-Pugh评分为7的亚组中,Namodenoson组的1年生存率达到了44%,显著高于安慰剂组的18%,中位总生存期和中位无进展生存期也都有高于安慰剂组的趋势。
Child-Pugh评分为7的患者中,namodenoson组的1年生存率显著更高
另外,试验中有55名患者进行了反应评估。Namodenoson组进行了评估的34名患者中,3人部分缓解,17人疾病稳定,客观缓解率8.8%,疾病控制率58.8%。而安慰剂组参与评估的21名患者只有10人达到了疾病稳定,客观缓解率0%,疾病控制率47.6%。
安全性上,Namodenoson的表现相当良好,不良反应的发生率与安慰剂相当。试验中没有因Namodenoson导致的死亡、停药或剂量减少事件,Namodenoson的治疗也没有产生肝毒性或肝功能异常。整个研究期间,Namodenoson导致的3级及以上不良反应只有1起3级的低钠血症。
目前,Namodenoson已经获得了FDA授予的孤儿药资格和快速通道资格,正在进行III期临床研究。
Can-Fite的首席执行官Pnina Fishman博士表示:“我们致力于在临床试验中为这一(Child-Pugh B)患者人群提供具有出色安全性和强大疗效的Namodenoson,以满足迫切的医疗需求。Namodenoson的抗癌作用和肝脏保护特性使其在针对这种严重疾病的抗癌药物中独树一帜。”
[1]. https://ir.canfite.com/news-events/press-releases/detail/997/can-fites-drug-namodenoson-approved-for-compassionate
[2]. Granito A, Bolondi L. Non-transplant therapies for patients with hepatocellular carcinoma and Child-Pugh-Turcotte class B cirrhosis[J]. The Lancet Oncology, 2017, 18(2): e101-e112.
[3]. Hollebecque A, Cattan S, Romano O, et al. Safety and efficacy of sorafenib in hepatocellular carcinoma: the impact of the Child‐Pugh score[J]. Alimentary pharmacology & therapeutics, 2011, 34(10): 1193-1201.
[4]. Cohen S, Stemmer S M, Zozulya G, et al. CF102 an A3 adenosine receptor agonist mediates anti‐tumor and anti‐inflammatory effects in the liver[J]. Journal of cellular physiology, 2011, 226(9): 2438-2447.
[5]. Stemmer S M, Manojlovic N S, Marinca M V, et al. Namodenoson in advanced hepatocellular carcinoma and child–pugh B cirrhosis: Randomized placebo-controlled clinical trial[J]. Cancers, 2021, 13(2): 187.







.jpg-pd13)

.jpg-pd13)


-scaled-e1698827217272.jpg-pd13)












 X
X