2020年5月15日,美国FDA基于CheckMate227研究1a部分,批准纳武利尤单抗联合伊匹木单抗用于转移性NSCLC成人患者(PD-L1≥1%且无EGFR或ALK基因突变)的治疗。
该适应症成为全球首个肺癌一线治疗的双免疗法。

2022年10月12日,在Journal of Clinical Oncology(IF 50.7)杂志,该研究正式发表,标题为“Five-Year Survival Outcomes With Nivolumab Plus Ipilimumab Versus Chemotherapy as First-Line Treatment for Metastatic Non-Small Cell Lung Cancer in CheckMate 227”。
研究结果显示
纳武单抗联合伊匹木单抗与化疗比,显著延长了非小细胞肺癌5年生存率。
并且,纳武单抗联合伊匹木单抗因治疗相关不良事件停药后,生存获益继续存在,5年OS率为39%(PD-L1≥1%和<1%人群)。

本研究共纳入了1739位无EGFR突变或ALK改变的IV期/复发性NSCLC患者。
根据PD-L1的表达结果:
-
肿瘤PD-L1≥1%的患者(n=1189)被分别随机分组到纳武利尤单抗+伊匹木单抗(n=391)、纳武利尤单抗单药治疗(n=391)或化疗(n=387)一线治疗;
-
肿瘤PD-L1 <1%的患者(n=550)被随机分组到纳武利尤单抗+伊匹木单抗(n=185)、纳武利尤单抗+化疗(n=172)或化疗(n=183)。
研究终点包括疗效、安全性和生活质量(QoL)的探索性5年结果。

研究结果:
1. 在至少61.3个月随访时
PD-L1≥1%组:纳武利尤单抗+伊匹木单抗组与化疗组的5年OS率分别为24%和14%。中位持续缓解时间分别为24.5个月和6.7个月。
PD-L1 <1%组:纳武利尤单抗+伊匹木单抗组与化疗组的5年OS率分别为19%和7%。中位持续缓解时间分别为19.4个月和4.8个月。
2. 完成2年免疫治疗的患者的疗效
133(12%)位患者完成了两年免疫治疗(PD-L1≥1%:13%完成纳武利尤单抗联合伊匹木单抗,11%完成纳武利尤单抗)。PD-L1<1%:9%完成纳武利尤单抗联合伊匹木单抗,13%完成纳武利尤单抗联合化疗)。
-
PD-L1≥1%组:纳武利尤单抗联合伊匹木单抗和纳武利尤单抗单药的五年OS率均为72%。
-
PD-L1<1%组:纳武利尤单抗联合伊匹木单抗五年OS率56%,纳武利尤单抗联合化疗五年OS率64%。
-
PD-L1≥1%组和PD-L1分别<1% 组中,纳武利尤单抗联合伊匹木单抗ORR分别为88%和94%。
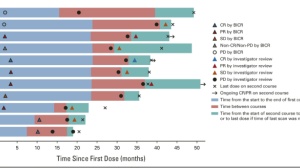
在存活5年的患者中,截至5年时间点,66% (PD-L1≥1%)和64% (PD-L1 <1%)已停止纳武利尤单抗+伊匹木单抗治疗,并且没有后续全身性抗癌治疗。
3. 因治疗相关不良事件停用的患者的疗效
在PD-L1≥1%组和PD-L1分别<1% 组中分别有17%和8%的患者因治疗相关不良事件停用纳武利尤单抗+伊匹木单抗治疗。因治疗相关不良事件停用纳武利尤单抗联合伊匹木单抗后,生存获益继续,5年OS率为39%(包含了PD-L1≥1%和<1%人群)。

安全性数据方面:通过5年随访,纳武利尤单抗联合伊匹木单抗治疗的5年生存者的QoL与美国一般人群相似,未观察到新的安全性信号。
总结
1. PD-L1≥1%组:纳武利尤单抗+伊匹木单抗组与化疗组的5年OS率分别为24%和14%,中位持续缓解时间分别为24.5个月和6.7个月。
2. PD-L1 <1%组:纳武利尤单抗+伊匹木单抗组与化疗组的5年OS率分别为19%和7%。中位持续缓解时间分别为19.4个月和4.8个月。
3. 截至5年时间点,超60%患者已停止纳武利尤单抗+伊匹木单抗治疗,并且没有后续全身性抗癌治疗。
4. 因治疗相关不良事件停用纳武利尤单抗+伊匹木单抗后,生存获益继续,5年OS率为39%。
5. 纳武利尤单抗+伊匹木单抗治疗的5年生存者的QoL与美国一般人群相似。
本文仅供医学药学专业人士阅读




.jpg-pd13)





.jpg-pd13)













 X
X