新一代ALK抑制剂Brigatinib能够穿透ALK阳性NSCLC患者的血脑屏障,取得较好颅内疗效。
《JCO》上发表了一篇文章,探索性分析了Brigatinib I/II期研究和II期ALTA研究中,基线合并脑转移患者的疗效。
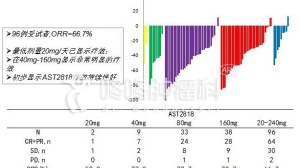
结果显示:Brigatinib用于既往接受过克唑替尼治疗的,合并脑转移的ALK阳性NSCLC患者,可以取得较好的颅内ORR(53%-67%)以及持久的iPFS(14.6-18.4个月)。
NSCLC患者中的ALK基因重排的发生率约为3-7%,临床上常见于不吸烟的年轻腺癌患者,通常与 EGFR 或KRAS 突变的发生互相排斥。
克唑替尼已被批准用于治疗ALK阳性晚期NSCLC。随后,塞瑞替尼、阿雷替尼和Brigatinib这三个二代ALK抑制剂陆续获批。
2018年5月31日,塞瑞替尼正式在国内获批,中位PFS16.6个月。
今天的主角是Brigatinib。
对于ALK阳性的NSCLC,约30%的初治患者合并脑转移,接受克唑替尼进展后的患者,60%合并CNS转移。
塞瑞替尼和阿雷替尼用于ALK阳性患者一线治疗可以延缓CNS转移的发生。此外,在克唑替尼耐药后的患者也能很好的控制CNS疾病。
在所有获批的二代ALK抑制剂中,Brigatinib是第一个用于克唑替尼耐药患者中能取得12个月PFS(无进展生存期)的药物,因此,Brigatinib的颅内疗效成为大家关注的热点。

近期在《JCO》杂志上,Camidge教授等发表的一项探索性分析,入组了Brigatinib I/II期研究和II期ALTA研究中,基线合并脑转移患者的疗效,研究中患者接受Brigatinib 90mg/天或180mg/天(首剂90mg/天)治疗。
在I/II期研究和ALTA研究中,分别纳入50例和153例基线合并脑转移的患者,其中50-60%的患者既往接受过靶向放疗,此外,ALTA研究中70%的患者既往接受过全脑放疗。研究者评估了颅内ORR和颅内PFS(iPFS),要求颅内转移灶的大小>=10mm才可以进行疗效平均,因此I/II期研究和ALTA研究中分别只有15例和59例患者可评估疗效。
在I/II期研究中,15例患者颅内靶病灶既往接受过放疗,未确认进展,接受Brigatinib治疗确认的颅内ORR为53%,iPFS为14.6m;在ALTA研究中,要求接受过放疗的颅内靶病灶进展。
结果显示,接受Brigatinib 90mg/天治疗的26例患者,颅内ORR为46%,iPFS为15.6m;接受Brigatinib 180mg/天治疗的18例患者,颅内ORR为67%,iPFS为18.4m。

基于上述结果可以看出,无论患者既往是否接受过克唑替尼治疗,Brigatinib 均可以很好进入CNS。
在克唑替尼耐药的患者中,可以取得67%的ORR和18.4个月的iPFS,尤其强烈支持Brigatinib 180mg/天用于合并脑转移的患者。
此外,大多数患者对Brigatinib的耐受性好,最常见不良事件(AE)包括恶心、腹泻、头痛和咳嗽,以及9%的早期肺毒性,
随着新一代ALK TKI的问世,CNS不再是ALK阳性患者的避难所。
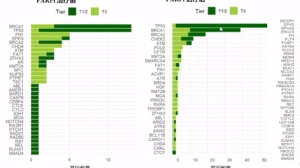
一线克唑替尼治疗进展的患者,后续可以根据患者特定的耐药突变,选择接受Brigatinib或其他ALK TKI治疗,ALK TKI的耐药机制较为复杂,包括ALK扩增,二次突变,旁路激活等,可以通过对耐药后的组织或液体活检标本检测来探寻耐药机制,此外,近期一些研究提示,基于ALK融合变体亚型预测患者的可能的耐药机制。
随着新一代ALK TKI的问世,ALK阳性NSCLC患者的长期生存成为可能。
参考文献:Infiltrating the Blood-Brain Barrier in ALK-Positive Lung Cancer.
本文仅供医学药学专业人士阅读




.jpg-pd13)



-1.jpg-pd13)
-1-scaled.jpg-pd13)
.jpg-pd13)












 X
X