胃癌是紧随肺癌其后的,全球第二大癌症死亡原因。
转移性胃癌5年生存率极低。临床试验证明,联合化疗药物治疗要比单药治疗延长总生存期。但是,胃癌的靶向治疗始终停滞不前。目前FDA只批准了两个靶向药物用于胃癌治疗,一个是抗血管生成药物雷莫芦单抗,另一个是针对Her2阳性胃癌的曲妥珠单抗赫赛汀,且这两种药物对于胃癌的总生存期帮助有限。
另一方面,在过去的10年里,免疫治疗在多种肿瘤治疗中表现出显著的优势。而且很多种药物逐渐被批准用于各自具有治疗优势的癌种。这些药物包括CTLA-4抗体ipilimumab,PD-1抗体K药和O药,以及PD-L1抗体T药(atezolizumab),B药(avelumab)和I药(durvalumab)。
尽管临床试验有一定的有效率,但是还没有一种免疫治疗药物被批准用于胃癌的治疗(除了K药被批准用于治疗MSI-H型的各种肿瘤,当然包括MSI-H型的胃癌)。近来公布了结果的临床试验表明:
- K药对于259名晚期胃癌的总体有效率为11.2%,其中PD-L1阳性患者的有效率为15.5%,而PD-L1阴性患者的有效率只有5.5%;
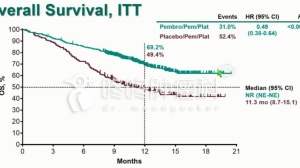
- 而在O药治疗晚期胃癌的III期临床试验中,虽然O药降低了37%的死亡风险,但O药中位无病生存期只有1.61个月,安慰剂的中位无病生存期为1.45个月。
寻找有效地标志物去判断和预测哪些人对免疫治疗有效是当务之急。然而目前的预测标志物诸如PD-L1的表达,TMB等都有其局限之处,也就是说预测可能并不准确。我们不时可以看到PD-L1阳性的无效患者和PD-L1阴性的有效案例。
今天我们要分享的是一个MSS胃癌患者的故事,她没有POLE突变,TMB很低,但是PD-L1抗体治疗后,全身肿瘤几乎完全消失。
患者是一名53岁的女性,因吐血而行胃镜检查,并确诊为低分化的EGFR无扩增的淋巴上皮瘤样的胃腺癌。
经确认无远端脏器转移后,患者接受了术前辅助化疗,然后进行了手术。术后病理肿瘤7厘米,手术切缘阳性,22枚淋巴结里有21枚有癌转移。患者被诊断为IIIC期。术后患者进行了放疗和化疗。
16个月后,PET显示局部和远端淋巴结转移,食道转移。患者接受了顺铂联合伊立替康化疗,有一定疗效。
7个月后,治疗方案换成了紫杉醇联合雷莫芦单抗。
15个月后,患者出现了严重的吞咽困难,影像学检查证实患者食道的转移和淋巴结转移均有进展,而且因为不能经口进食而住院治疗并放置了空肠营养管。
之后,患者被推荐去新泽西州参与PD-L1抗体B药的临床试验,接受了10mg/kg的B药每两周一次治疗。在第一次复查时,患者食道和淋巴结的转移就明显好转。随着治疗的继续,患者吞咽困难逐渐改善,食道转移瘤缩小,肿大淋巴结消失。
患者接受了多于24次的治疗(即B药的效果持续至少1年)。但是这位患者的肿瘤组织基因分析为MMR/MSS,TMB低,POLE无突变,这些标志物都是我们经常认为免疫治疗无效的征兆。不过,患者具有PIK3CA和ARID1A突变。这两个突变常在EB病毒阳性的胃癌中出现。所以研究者检查了患者肿瘤中的EB病毒,并证实患者为感染了EB病毒的胃癌分型。而且患者的肿瘤是PD-L1阳性,并在相同区域有免疫细胞浸润。

患者EB病毒感染阳性,而且肿瘤组织中众多的淋巴细胞浸润,肿瘤细胞和浸润的淋巴细胞上都有PD-L1高表达。
研究者并没有就此停下探索。研究者们开始在癌症基因组图谱数据库中查找胃癌基因表达和突变的信息,以期能够从一个患者的特殊情况扩展到更多的胃癌患者。研究者们发现:
因此,研究者认为,从这一个案例报告和他们对胃癌基因数据库的发掘可以得出,EB病毒阳性的MSS型胃癌作为一个胃癌的特殊分组或许可以从免疫治疗中获益。
当然,这个发现还有待于进一步的大型临床试验来验证。我们在这里提醒胃癌患者,不妨用组织切片做一下EB病毒的检测,或许你也会是一个PD-L1抗体的超级响应者。
除了胃癌,EB病毒感染常见于鼻咽癌(90%以上的鼻咽癌)以及各类淋巴瘤(尤其是伯基特淋巴瘤、NK/T细胞淋巴瘤以及部分非霍奇金淋巴瘤)——这些病友,都可以检测一下PD-L1表达。
参考文献:
Immune Activation and Benefit From Avelumab in EBV-Positive Gastric Cancer.J Natl Cancer Inst. 2018 Mar 1;110(3):316-320.
本文仅供医学药学专业人士阅读





-1.jpg-pd13)
-1-scaled.jpg-pd13)
.jpg-pd13)












 X
X