
一、胸腔积液的诊疗介绍 ………………. P2
二、恶性胸腔积液(MPE)诊断与治疗专家共识 ………….P3
三、恶性胸腔积液诊断与治疗现状及进展 ……………. P6
四、遏制非小细胞肺癌恶性胸腔积液有新招 ………….. P8
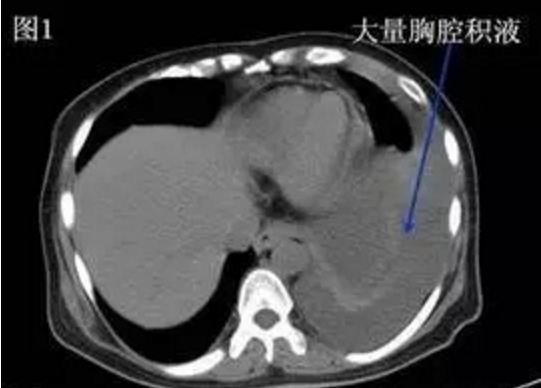

一、胸腔积液的诊疗介绍
胸腔积液:任何原因导致胸膜腔内出现过度的液体称胸腔积液。
分类:
性质分类
漏出液、渗出液、脓胸、血胸、乳糜胸。
病因分类
肺梗死、血管瘤破裂、胸导管破裂受阻、食管疼;全身性:低蛋白血症、肝肾病综合征;其它疾患:腹膜透析、粘液性水肿、放射反应;创伤性:胸部手术后、胸部外伤。
今天我们主要从呼吸相关的胸腔积液进行讨论
胸水的发生机制
健康人的胸膜腔壁层与脏层胸膜之间存在着一个潜在的腔隙,其中含有少量润滑液,大约30~50ml。过去认为每天有数升胸腔积液循环于胸腔。近年研究证实,在正常情况下每天产生100~200ml胸液。
胸腔积液形成的主要原因
胸内淋巴系统引流障碍:壁层胸膜小孔被堵塞,纵膈淋巴结受压或淋巴管栓塞,以上两者同时存在。
临床表现
结核性胸膜炎:多见于青年人,常伴结核中毒症状;肺癌转移:多发生于中年以上患者,其它症状不典型;感染性积液:常伴有胸痛及发热;漏出性积液:常伴有胸痛及发热;漏出性积液:心力衰竭症状、低蛋白的表现
也可根据积液的性质和量的不同而不同,积液<300 ml,可无症状;中等量或大量时呼吸困难明显,患侧呼吸运动减弱,语颤消失,积液叩诊实音,听诊呼吸音减弱或消失,纵隔移向健侧;大量积液时纵隔脏器受压,心脏呼吸困难更加明显。
胸水的常规检查
包括胸水外观、胸水的PH、胸水细胞
胸水生化
蛋白质、类脂、葡萄糖、酶、淀粉酶、腺苷脱氨酶(ADA)
免疫学检查
结核性与恶性胸腔积液时,T淋巴细胞增高;尤以结核性胸膜炎为显著可高达90%,且以T4(CD+4)为主;恶性胸腔积液中的T细胞功能受抑,其对自体肿瘤细胞的杀伤活性明显较外周血淋巴细胞为低,示恶性胸腔积液患者胸腔内局部免疫功能呈抑制状态。
与肿瘤分子靶向治疗有关的检查
胸水游离DANA进行EGFR/KRAS/BRAF/PI3K等基因突变检查;胸水中的肿瘤细胞进行免疫组织化学ALK的D5F3检查;用比较基因组杂交技术(FISH)进行ALK/ROSI/C-MET融合突变的检查。
胸膜活检
经皮胸膜活检对鉴别有无肿瘤及判定胸膜肉芽肿性病变有一定帮助;拟诊结核病时,活检标本除作病理检查外,尚可作结核菌培养;脓胸或有出血倾向者不宜做胸膜活检,必要时可经胸腔镜进行活检。
若胸膜病变范围较广,使葡萄糖及酸性代谢产物难以透过胸膜,可使葡萄糖含量较低,提示肿瘤可能广泛浸润,
目前诊断金标准是B超,B超的胸水定位。但在B超在拿不准的情况下,进行CT检查。
已经诊断明确后就应该针对不同的情况进行治疗
少量胸液一般不必抽液或仅作诊断性穿刺;抽液后可减轻毒性症状,体温下降,有助于使被压迫的肺迅速复张;可解除肺及心、血管受压,改善呼吸,阻止纤维蛋白沉着与胸膜增厚,使肺功能免受损伤;大量胸液者每周抽液2-3次,直到胸液完全吸收。或置管持续引流。
结核性胸腔积液的糖皮质激素的使用
可减少机体的变态反应及炎症反应;改善毒性症状,加速胸液吸收,减少胸膜粘连或胸膜增厚等后遗症;但亦有一定不良反应或导致结核播散,故应慎重掌握适应症。
脓胸
指由各种病原微生物引起的胸膜腔感染性炎症,同时伴有外观浑浊,具有脓样特征的胸腔渗出液;细菌是脓胸的最常见病原体;大多数细菌性脓胸与细菌性胸膜炎未能有效控制有关;少数脓胸可由结核菌或真菌、放线菌、奴卡菌所致。
恶性胸腔积液
以渗出性胸膜炎最为常见;中老年胸腔积液(尤其是血性胸液)应慎重考虑恶性病变与恶性肿瘤(如肺癌、乳腺癌、淋巴瘤等)向胸膜活纵隔淋巴结转移,可引起胸腔积液;肿瘤累及胸膜,使其表面通透性增加,或淋巴引流受阻,或伴有阻塞性肺炎累及胸膜,均可引起渗出性胸腔积液;偶因胸导管受阻,形成乳糜胸。
肺癌胸腔积液
全身化疗对于部分小细胞肺癌所致胸腔积液有一定疗效;纵隔淋巴结有转移者可行局部放射治疗;在抽吸胸液后,胸腔内注入包括阿霉素、顺铂、氟尿嘧啶、丝裂霉素、硝卡芒芥、博来霉素等在内的抗肿瘤药物,是常用的治疗方法,有助于杀伤肿瘤细胞、减缓胸液的产生,并可以引起胸膜粘连。
二、恶性胸腔积液(MPE)诊断与治疗专家共识
几乎所有类型的恶性肿瘤发展至晚期均会出现恶性胸腔积液(MPE)。近期,我国“恶性胸腔积液诊断与治疗专家共识”公布,其由施焕中教授发起,经过我国20多位著名专家多次修改,历时半年多才最终定稿。该共识汇聚了文献精华和专家经验,对恶性胸腔积液的临床诊断和治疗具有指导意义。
诊断:病理学检查是金标准
确定MPE诊断的“金标准”仍是在胸水细胞沉淀中找到恶性细胞,或在胸膜活检组织中观察到恶性肿瘤的病理变化。
临床表现
可作为诊断MPE的重要线索。大部分MPE患者有临床症状,但约25%患者可表现为无症状,经体检或胸部X线检查偶然发现。
影像学检查
大多MPE患者胸部X线检查均能观察到中等量至大量胸水,一般为500-2000ml,约10%患者表现为大量胸水,约15%患者胸水<500 ml。计算机断层扫描( CT)有助于发现少量MPE,判断是否伴有纵隔淋巴结转移,对潜在肺实质病变进行评估。磁共振成像(MRI)对MPE的诊断价值有限,但可能有助于评估肿瘤侵袭纵隔或胸壁范围。初步研究显示,氟脱氧葡萄糖正电子发射CT扫描对MPE具有良好预测价值,但有待更多循证医学证据支持。
诊断性胸腔穿刺术
行胸腔穿刺无绝对禁忌证,相对禁忌证包括胸水量过少(单侧卧位胸水平面距离胸壁<1 cm)、出血倾向、正在接受抗凝治疗和机械通气等。绝大多数MPE为渗出液,细胞分类以淋巴细胞为主;但也有极少数是漏出液。
胸水细胞学是诊断MPE的最简单方法,多次检查可提高阳性率。某些肿瘤标志物如癌胚抗原、细胞角蛋白片段21-1、糖类抗原有助于MPE诊断。联合检测多种标志物可提高诊断效率。
闭式胸膜活检术
对MPE诊断的敏感度低于细胞学检查,诊断率为40%~75%。若CT发现胸膜异常(如间皮瘤),建议在超声或CT引导下行经皮闭式胸膜活检。
内科胸腔镜检查术
主要用于不明原因渗出性胸腔积液的鉴别诊断;也可通过内科胸腔镜喷洒滑石粉行胸膜固定术治疗MPE。内科胸腔镜检查可获取更大、更具有代表性的病变组织,因此比闭式胸膜活检术更利于对胸膜恶性肿瘤作出较早期诊断、组织学分类及临床分期。
外科活检术
可采用胸腔镜或开胸两种方式。外科胸腔镜活检术通常要求全身麻醉和双腔气管插管,由于术中单侧肺通气,因此外科胸腔镜可视范围比内科胸腔镜广阔,可同时进行诊断与治疗操作。患者不能耐受单肺通气是外科胸腔镜活检术的禁忌证,此时应考虑开胸活检术。
支气管镜检查术
当怀疑存在肺内占位、出血、肺膨胀不全、支气管黏膜病变或大量胸水无纵隔移位时,应行支气管镜检查术。
[解读]
并非所有恶性肿瘤患者的胸腔积液均是恶性,有可能为肿瘤旁胸腔积液,这部分患者胸腔积液中不存在恶性细胞,胸膜也无转移瘤。有研究表明,出现胸腔积液的肺癌患者中仍有5%患者有手术机会。因此,在诊断和鉴别诊断恶性肿瘤并发胸腔积液时,尤其应慎重对待胸腔积液中细胞学检查结果为阴性的患者,只要无胸膜及其他部位转移证据,结合其他情况,有手术条件时应施行手术。
治疗:尽早考虑姑息治疗
MPE诊断一旦明确,应尽早考虑姑息治疗。对患者的症状、一般情况及预期生存时间进行全面评估,然后再制定治疗方案。治疗的主要目的是减轻呼吸困难症状。
临床观察
是指针对MPE本身不做任何治疗干预,推荐用于原发肿瘤已明确但无症状的MPE患者。对有症状的MPE患者,需咨询呼吸科专科医生的意见,决定是否采取单纯的观察。
治疗性胸腔穿刺术
胸腔穿刺排液后1个月内MPE复发率较高,因此不推荐用于预期寿命超过1个月者。反复行治疗性胸腔穿刺术可暂时缓解呼吸困难,使部分预期生存时间短、体能状况差者避免住院,适用于体质虚弱和终末期患者。
肋间置管引流及胸膜固定术
对预期寿命极短的患者一般不推荐反复行胸腔穿刺术,可于肋间置入小口径引流管引流胸水,以缓解呼吸困难症状。如肺脏无明显萎陷,肋间置管引流后应行胸膜固定术以防止MPE复发。单纯肋间置管引流术而不实施胸膜固定术者MPE复发率高,故应避免单纯行肋间置管引流术。
临床上,施行肋间置管引流及胸膜固定术应注意一些事项(图1)。
门诊长期留置胸腔引流管
留置胸腔引流管是控制复发性MPE的一种有效方法,尤其是对肺萎陷或希望缩短住院时间的患者。每隔一段时间将导管与真空引流瓶连接进行引流,可促进肺复张和胸腔闭锁,大多数引流管短期留置后可拔除。
胸腔内注射纤维蛋白溶解剂
对于多房性MPE、单纯引流效果不佳者,推荐胸腔内注射纤维蛋白溶解剂如尿激酶、链激酶等减轻胸膜粘连、改善MPE引流以缓解呼吸困难症状。
经胸腔镜治疗
对体能状况良好者,推荐经胸腔镜治疗用于可疑MPE的诊断,也推荐用于已确诊MPE者行胸水引流及胸膜固定术。
其他
(1)全身治疗:某些肿瘤(如小细胞肺癌)胸膜转移所致的MPE,可能对化疗有较好的反应,如无禁忌证可考虑全身治疗,同时联合胸腔穿刺或胸膜固定术。(2)外科治疗:由于目前循证医学证据不充分,暂不推荐应用胸膜切除术替代胸膜固定术或留置胸腔导管治疗复发性胸水或肺萎陷。(3)胸腔内治疗:目前尚无足够的循证医学证据支持胸腔内治疗。
[解读]
目前,几乎所有针对MPE的姑息性干预手段均存在缺陷,无法取得满意疗效,且只适用于部分患者。
治疗MPE的理想方法是能迅速缓解患者的症状,作用持久,无需反复操作。因患者的预期生存时间只有数月,应尽可能选择创伤小、不引起明显不适、并发症少而轻微的治疗手段。此外,还要考虑MPE的管理尽可能不影响针对原发肿瘤的处理,最好能在门诊就能进行操作,能减轻患者及家属的负担。
三、恶性胸腔积液诊断与治疗现状及进展
导语:恶性胸腔积液(MPE)是肿瘤晚期最常见的并发症之一,也可作为恶性肿瘤的首发症状出现,或是肿瘤治疗后复发的症状。MPE可来源于原发胸膜的恶性肿瘤,胸腔内肿瘤,或胸腔外肿瘤通过血道转移、淋巴道转移或直接播散转移。
尽管所有的恶性肿瘤均可引起MPE,统计结果表明,约有75%是来源于肺癌、乳腺癌、卵巢癌及淋巴瘤,约7%找不到原发病灶。转移性腺癌为最常见的病理类型,原发胸膜的MPE为恶性间皮瘤。
无论恶性胸腔积液来源于何,一旦发现提示,患者预后不良,生存期一般小于6个月,且严重影响患者生活质量。因此,正确诊断并有效控制MPE有着重要的临床意义。
恶性胸腹腔积液的发生机制
正常情况下,胸腔和腹膜腔内都有少量的液体在起着润滑作用,其产生和吸收处于一种平衡状态。恶性胸腔积液定义为胸腔内出现肿瘤细胞。
转移性MPE一般由于临近肿瘤如肺癌、乳腺癌和胸壁恶性肿瘤的直接浸润。肿瘤癌栓使脏层胸膜功能障碍,或肿瘤通过血道转移至脏层胸膜,使胸膜腔积液的回流吸收受阻出现胸腔积液。
若侵犯淋巴结造成淋巴管的破坏,还可产生乳糜胸;血管内皮生长因子介导的使毛细血管的通透性增加,也是恶性胸膜腔积液产生的原因之一。
肿瘤患者胸腔内无肿瘤细胞,但有非肿瘤直接导致的胸腔积液,如纵隔肿瘤浸润、支气管堵塞、放疗、肺梗死及上腔静脉综合征等,称为“类恶性胸腔积液”。20%~30%的非霍奇金恶性淋巴瘤和霍奇金恶性淋巴瘤伴有胸腔积液。大多数的霍奇金淋巴瘤为“类恶性胸腔积液”,原因是胸导管堵塞;大多数的非霍奇金淋巴瘤伴有胸腔积液为T细胞类型,是由于肿瘤直接浸润胸膜引起。
恶性胸腔积液诊断
MPE的诊断一般通过患者的病史、体检、胸腔积液的生化检查、细胞病理学检查以及影像学检查来确定。患者常出现气短、咳嗽以及活动受限等症状。大多数来源腺癌的MPE无胸痛,而60%的胸膜间皮瘤患者伴有持续性胸部钝痛或局限性胸痛。
影像学检查
X线侧位摄片可检测50 ml胸腔积液,表现为肋膈角消失,半月形沿胸壁阴影。大量胸腔积液可表现为纵膈向对侧移位。
胸部超声检查可检测到5ml的胸腔积液,并可作为胸腔穿刺或置管定位,表现为低回声胸膜增厚,界限常不规则,有时因胸腔积液含有细胞碎片而不均匀。
怀疑MPE时应进行胸部、肾上腺及肝脏的CT检查,寻找肿瘤原发病灶及明确肿瘤转移范围。CT诊断特异性为22% ~56%,敏感性为88% ~100%,具体表现有胸膜环形增厚,胸膜呈结节样改变,脏层胸膜增厚大于25px和纵膈胸膜受侵等。
胸膜间皮瘤表现有叶间胸膜受累,胸膜广泛增厚,可呈“波浪形”结节,有时可合并钙化。
胸腔积液检查分析
目前,超声定位指导下行胸腔穿刺或置管引流胸腔积液后进行生化及脱落细胞学检查为常规检查。
恶性胸腔积液主要为渗出液,国外使用的“LIGHT”标准包括LDH、胆固醇及蛋白含量的检测。
恶性积液细胞计数常大于50%(大于85%提示结核性胸膜炎、结节病或淋巴瘤),红细胞及嗜酸性粒细胞增多。生化检查蛋白增加(>3g/L),LDH增高(>1000U/L),pH值及糖含量降低等。
胸腔积液中肿瘤标志物如CEA、CA125、CA199、DNA异倍体等检测对诊断可提供一定帮助。
胸膜活检术
对胸腔积液检查未得到细胞学证实的患者可考虑应用胸膜活检。应用Abrams胸膜活检针的报道称,其诊断胸膜间皮瘤特异性为31%,腺癌为69%。应用CT或超声引导下的胸膜活检,敏感性可达86%~100%,特异性达100%。
外科和内科胸腔镜的胸膜活检术近年来也逐渐应用于临床。
恶性胸腹腔积液治疗
穿刺放液和腔内置管闭式引流
胸腔穿刺术放液简单、快速、安全,但对晚期肿瘤患者此法只能缓解症状72小时,需重复穿刺。
胸腔置管闭式引流术是在胸腔穿刺的基础上,将引流管置入胸腹腔,外接引流袋引流积液。这种方法减少穿刺次数,利于后续的腔内注药,是目前临床常用方法。
药物治疗
药物治疗是目前恶性胸腹腔积液最主要的方法。全身给药达到局部的药物浓度低,效果不佳。局部用药能达到较高的药物浓度,毒副反应小,因此更为常用。腔内应用的药物主要有:
硬化剂:向胸腹腔注入硬化剂会引起炎症反应、促进纤维蛋白沉积,使脏壁层胸膜粘连,从而控制胸腔积液生长。常用滑石粉、四环素及其衍生物、肿瘤坏死因子、干扰素、白介素-2等。主要不良反应有高热、疼痛、急性呼吸窘迫综合征等。2010年BTS指南指出,在使用硬化剂之前,可用利多卡因3mg/kg(最多250mg)腔内注射缓解疼痛。
化疗药物:常用铂类、氟尿嘧啶、博来霉素、阿霉素及依托泊苷等。报道称顺铂联合热灌注治疗肺癌引起的胸腔积液有效率达83%,患者耐受性良好。
生物反应调节剂:常用白介素、香菇多糖、沙培林、高聚金葡素、胞必佳等。报道称IL-2治疗胸腔积液总有效率为76.7%,IL-2联合顺铂治疗恶性胸、腹腔和心包积液的有效率达92.3%。
注:IL-2即白细胞介素-2(interleukin-2,IL-2),又名T细胞生长因子(T cell growth factor,TCRF)。主要由活化的CD4+Th1细胞产生的具有广泛生物活性的细胞因子。可促进th0和CTL的增殖,故为调控免疫应答的重要因子,也参与抗体反应、造血和肿瘤监视。环孢素、他克莫司等免疫抑制剂可以抑制其活性和生成。21世纪初人类开始的生命方舟计划对于IL-2的研究取得了突破性的进展。
中药制剂:常用榄香烯乳、华蟾素、鸦胆子油乳、康莱特等。报道单用榄香烯胸腔内注射治疗胸腔积液有效率为77.6%。
基因治疗:50%以上恶性肿瘤发生发展与p53基因的异常表达有关。研究者观察重组人p53腺病毒联合顺铂腔内注入治疗进展性恶性胸腹腔积液,有效率63%。
抗肿瘤新生血管药物:VEGF在恶性胸腔积液形成中起着重要的作用,报道称腔内应用抗VEGF抗体即贝伐单抗联合顺铂或单用顺铂治疗NSCLC引起的恶性胸腔积液,贝伐单 抗联合顺铂有效率为83%,而顺铂组为50%。
外科治疗
胸腔镜下胸膜固定术:内科胸腔镜和电视辅助胸腔镜外科手术(VATS)在胸膜固定术中均已广泛应用。多项研究表明,通过胸腔镜喷洒滑石粉剂治疗MPE的成功率在77%- 100%。
胸膜切除术及胸腔-腹腔分流术:胸膜切除手术病死率高(10%~19%),并发症包括脓胸、出血、呼吸循环衰竭等。胸腔-腹腔分流术(PVS)被用于治疗顽固性胸腔积液,患者会出现分流管腔堵塞、血栓等术后并发症。
小结
目前恶性胸腔积液的诊断及治疗已有了长足的发展,特别是影像检查、胸腔积液生化分析以及细胞病理学检查的进步。随着分子生物学的快速发展,特别是靶向药物为治疗恶性胸腔积液开辟了新的治疗手段。相信在不久的将来,新技术新药物一定可以为恶性胸腔积液患者带来更大的福音。
四、遏制非小细胞肺癌恶性胸腔积液有新招
解放军总医院第一附属医院肿瘤二科主任杜楠博士,对66名老年非小细胞肺癌恶性胸腔积液(MPE)患者,分别采用抗血管生成疗法联合胸腔内化疗,和单纯胸腔内化疗进行临床对照研究,发现这两种治疗方法的有效率分别为85.71%和56.67%,前者胸腔积液中血管内皮生长因子(VEGF)表达明显低于后者,没有出现不良反应。日前,相关研究论文在欧洲权威学术期刊《Onology Reports》(相关文献:2013 Jun 29)上发表。
非小细胞肺癌在肺癌中占75%~80%,其中50%以上的患者出现恶性胸腹腔积液,预后差,病死率高,中位生存期仅3个月~6个月。
长期以来,治疗恶性胸腹水主要采用反复穿刺抽液或胸腔注射化疗药物的方法,能在一定程度上减轻患者不适症状但不能改善生存质量,且反复抽液会导致体液蛋白质等营养物质大量丢失,导致病情恶化。
研究证实,恶性胸腹水的主要诱因是肿瘤新生血管生成和浆膜腔渗透压增高。而抗血管生成靶向药物贝伐珠单抗能直接抑制血管内皮细胞增殖、迁移、分化,促进内皮细胞凋亡,对抗血管内皮生长因子所致的促进新生血管形成和增加血管通透性,且能有效阻滞胸腔积液的产生,与化疗药物之间有很好的协同作用。
基于这样的认识,经解放军总医院伦理委员会批准,杜楠从2009年开始对晚期非小细胞肺癌合并胸腔积液患者采用抗血管生成疗法联合胸腔内化疗进行临床研究。
杜楠把72名66岁~82岁的患者随机分为腔内注射贝伐珠单抗联合顺铂化疗组和单纯腔内顺铂化疗组进行临床观察,在可评价的66名患者中, 贝伐珠单抗联合化疗组的总有效率为85.71%,单纯腔内化疗组为56.67%,两组疗效差异显著,且前者胸水中血管内皮生长因子表达明显低于后者,未出现严重不良反应,生活质量明显改善。5年来,他们采用这一疗法配合其他综合手段治疗非小细胞肺癌恶性胸水患者近300人。
本文仅供医学药学专业人士阅读










-1.jpg-pd13)
-1-scaled.jpg-pd13)
.jpg-pd13)












 X
X