3月9日,君实生物发布公告称其重组人源化抗PD-1单克隆抗体注射液(JS001)于近日正式获得CFDA的新药申请受理通知书。

JS001的中文名称正式亮相,为特瑞普利单抗。据君实生物负责人透露,此次获得受理的申请是JS001的新药上市申请,适应症为黑色素瘤。
JS001是国内企业首个获得CFDA 临床试验批件的抗 PD-1单克隆抗体注射液,目前正与国内多家临床中心开展黑色素瘤、鼻咽癌、胃癌、肺癌、食管癌、尿路上皮癌等10余个适应症 I~III 期临床试验。JS001于2018年1月获得FDA临床试验批准,是君实生物首个在全球开展临床试验的生物制品。
在ASCO2017大会上,君实公布过JS001的两项临床数据:
-
PD1单抗JS001治疗晚期癌症的I期临床结果。ASCO2017#e14581:入组了19例患者,15例患者可评估应答情况,1例霍奇金淋巴瘤完全应答,3例霍奇金淋巴瘤部分应答,1例软组织肉瘤部分应答,1例弥漫性大B细胞淋巴瘤部分应答。3级以上不良反应包括1例肺炎。
-
PD1单抗JS001治疗实体瘤的I期临床结果。ASCO2017#3067:入组36例患者(22例黑素瘤、9例尿路上皮细胞癌、5例肾细胞癌),32例患者可评价,1例黑素瘤完全应答,3例黑素瘤部分应答,2例肾细胞癌部分应答,1例尿路上皮细胞癌部分应答,另外10例患者疾病稳定。3级以上不良反应包括1例蛋白尿、2例脂肪酶升高。
特瑞普利单抗(JS001)是国内第4个提交上市申请的PD-1/PD-L1类药物。BMS的nivolumab已经在2017/11/2申报上市,用于二线治疗非小细胞肺癌,并获得了优先审评。信达生物的信迪单抗在2017/12/13提交上市申请,用于治疗霍奇金淋巴瘤。默沙东的帕博利珠单抗在2018/2/11提交了上市申请。
国产PD-1/PD-L1类药物的开发竞争也很激烈,目前已经有21个品种陆续向CDE提交了注册申请。
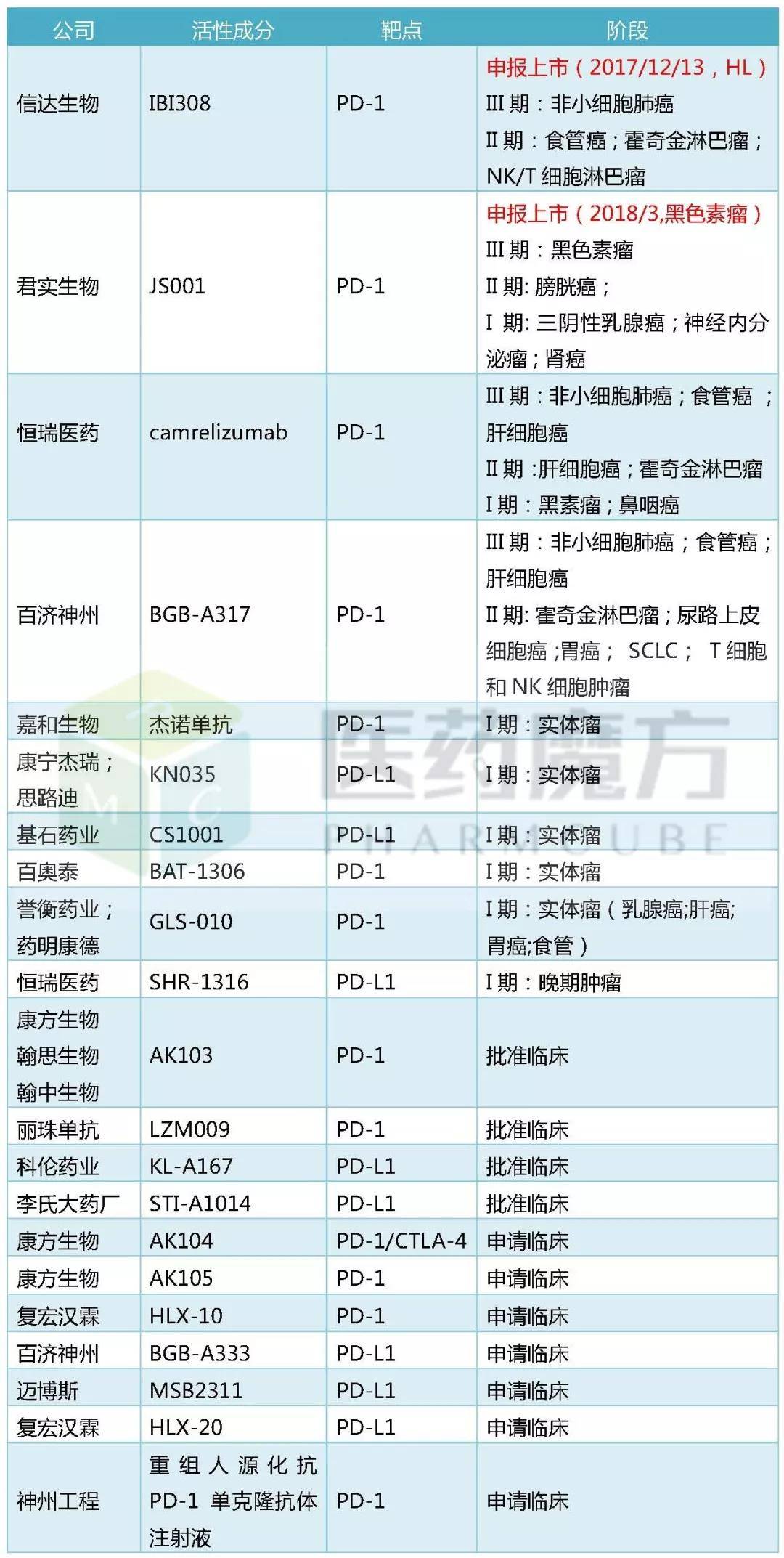 (内容转载自医药魔方微信公众号)
(内容转载自医药魔方微信公众号)
本文仅供医学药学专业人士阅读






















 X
X