肿瘤是分期的:I期、II期、III期、IV期;不同分期的肿瘤,治疗手段和治疗的目标是截然不同的。
一般早中期肿瘤以手术治疗为主,中晚期患者以放化疗、手术综合治疗为主,晚期的患者以药物治疗为主。
PD-1抗体、PD-L1抗体,均属于药物治疗,因此一直以来最常用的场景就是晚期癌症患者。
不过,随着临床研究的不断深入,免疫治疗正逐步扩展它的应用场景:
■ PD-L1抗体I药应用于III期肺癌同步放化疗后的巩固治疗,已经在国内外正式获批,I药用于III期肺癌在国内的第一张处方于今年的情人节(2月14日)正式开出;
■ PD-1抗体用于手术后高危的恶性黑色素瘤患者的辅助治疗,也早就在国外获得批准,大规模临床应用。近日,PD-1抗体K药用于三阴性乳腺癌手术前的新辅助治疗,大获成功,III期临床试验数据正式发表于《新英格兰医学》杂志,标准着免疫治疗用于实体瘤手术前的新辅助治疗,正式起航。
这样一来,PD-1/PD-L1抑制剂免疫治疗从难治性晚期患者的挽救治疗、晚期实体瘤患者的一线治疗、局部晚期患者根治性放化疗后的巩固治疗、中期患者手术后的辅助治疗,一直到早中期患者手术前的新辅助治疗,几乎全线贯通。
这也预示着在不久的将来,只要合理选择患者、精准安排治疗时机,免疫治疗几乎可以用于各大癌种、各种适应症。
新辅助治疗第一个获得成功的国际多中心三期临床试验,是Keynote-522临床研究。
这是一项原本计划入组约1000名临床分期是II-III期的三阴性乳腺癌患者的国际多中心临床试验。2:1分组,一组接受K药联合标准方案化疗,作为手术前的新辅助治疗,治疗结束后安排手术;另外一组接受标准方案的化疗作为新辅助治疗,治疗接受后安排手术。这项临床试验进展顺利,第一次初步分析的时候,对最早入组的602名患者的治疗结果进行了分析。
K药的加入,可以让肿瘤病例完全缓解率(从显微镜下仔细观察到找不到癌细胞,彻底的癌细胞消失)从51.2%提高到64.8%,足足抬高了13.6个百分点,具有显著的统计学差异。
该临床试验因为初步分析的结果太惊艳,提前胜利结束。中位随访15.5个月发现,K药的加入可以让疾病复发进展率从11.8%降低到7.4%。而且,K药加入其中的疗效提升,对几乎所有的病人,不管患者原发肿瘤的大小、是否有腋窝淋巴结转移、年龄高低以及PD-L1表达的高低,都可以从中获益。唯一获益不明显的患者,是那些体力体能情况较差的病友。
由于在三阴性乳腺癌中,手术前新辅助治疗导致的病理学完全缓解率和治愈率、患者生存期密切相关,病理学完全缓解率越高,后续规范治疗后治愈率越高、患者生存期越长。而K药的加入,大幅度提高了新辅助治疗的病理完全缓解率,而且绝大多数患者可以获益,这样的结果,基本是宣告了PD-1抗体正式揭开了新辅助治疗的序幕。
近期,这些癌种也有新的数据。
2020年2月,国家癌症中心的赫捷院士在《JTO》杂志上发表了合资PD-1抗体信迪利单抗用于非小细胞肺癌新辅助治疗的II期临床试验数据。40名患者入组,先接受两个疗程的PD-1抗体治疗,然后再安排手术。
8名患者在接受2个疗程PD-1抗体治疗后,肿瘤明显退缩。37名患者顺利接受了手术,其中15名患者病理学大部分缓解,6名患者病理学完全缓解。
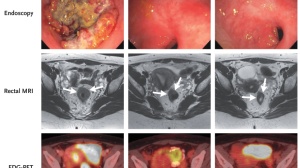
研究还发现:鳞癌患者疗效更好(近50%的患者达到了病理学缓解),PD-L1阳性的患者疗效更好;此外,他们发现在治疗前和2个疗程PD-1抗体治疗结束后分别做一次PET-CT,PET-CT上代谢值明显下降的患者,疗效好。

上个月,中山大学附属肿瘤防治中心的丁培荣教授报道了8例MSI阳性的结直肠癌患者,接受PD-1抗体新辅助治疗的结果:8例患者均实现了病理学显著的缓解,1例患者PD-1抗体治疗结束后影像学片子上已经看不到肿瘤,干脆拒绝手术,一直定期复查;另外7人接受了手术,其中4名患者显微镜下都找不到癌细胞了,达到了振奋人心的病理学完全缓解。
综上所述,趁着肿瘤还在早中期,患者体力体能评分也好,免疫状态也不错,尽早安排免疫新辅助治疗,或许会成为未来一段时间临床研究和临床探索的新时尚。
[1]. Pembrolizumabfor Early Triple-Negative Breast Cancer.NEngl J Med 2020;382:810-21
[2]. NeoadjuvantPD-1 inhibitor (Sintilimab) in Non-Small Cell Lung Cancer.https://doi.org/10.1016/j.jtho.2020.01.017
[3]. PD-1blockade in neoadjuvant setting of DNA mismatch repair-deficient/microsatelliteinstability-high colorectal cancer.https://doi.org/10.1080/2162402X.2020.1711650










.jpg-pd13)
.jpg-pd13)

















 X
X