肾癌靶向治疗药物的主要作用机制
靶向治疗是晚期肾癌的治疗手段之一,从作用机制方面主要分为两类:抗血管内皮生长因子(VEGF)/血管内皮生长因子受体(VEGFR)和抑制mTOR通路。
近年来,肿瘤治疗领域已经研发了多种具有抗血管生成靶向活性的药物,包括以抑制VEGF通路为主的舒尼替尼、索拉非尼、培唑帕尼、阿昔替尼和贝伐珠单抗,以及阻断下游mTOR通路的依维莫司和替西罗莫司等。多项针对靶向药物的国际大型临床研究的结果显示,靶向药物显著改善了晚期肾癌患者的生存。
其中,血管生成是肿瘤生长和生存的关键,这个过程通过促血管生成因子(如VEGF、PDGF、FGF)和抗血管生成因子(如血管抑素、内皮抑素、血小板反应蛋白等因子)形成平衡。而VEGFR和PDGFR信号均是血管生成的关键。VEGF是最重要的促血管生成因子,且事实上在所有实体肿瘤(特别是肾癌)中过度表达。另外,PDGF信号能够募集周细胞刺激肿瘤血管生成,有利于肿瘤血管的成熟、稳定和存活。因此,同时阻滞VEGF和PDGF通路可能在抑制肿瘤血管生存上较单一靶向VEGF通路更为有效。

在新型的肾癌靶向治疗药物当中,培唑帕尼于2009年10月获美国食品与药品管理局(FDA)批准上市,用于治疗肾细胞癌。其为一种新型的口服、强效和高选择性的多靶点酪氨酸激酶抑制剂,能够抑制调节血管生成相关的VEGFR-1、VEGFR-2 和VEGFR-3,调节血管生成和某些肿瘤细胞增殖的PDGFR-α、 PDGFR-β及调节细胞的增殖和生存的c-Kit细胞内酪氨酸激酶部分等多个靶点。临床研究表明,其对肾细胞癌的药效明显,安全性研究结果也表明患者耐受良好,该药为晚期肾细胞癌的治疗提供了新的选择。而其作为一个多靶点药物,为患者带来良好获益的同时,也有着一些独特的不良反应,现整理如下。
新型靶向药物培唑帕尼的安全性研究
在晚期肾细胞癌治疗中带来有效性的同时,TKI药物也与潜在的不良反应相关,其对患者生活质量、日常活动的能力、治疗的依从性等也将产生不良影响。快速、有效地识别和立即处理不良反应是十分重要的,以避免不必要的剂量降低,从而对疗效产生负面影响。
1、血液学毒性
既往研究证实,与肿瘤治疗相关的骨髓抑制可能会导致血液学异常,包括中性粒细胞减少、贫血、血小板降少等。而骨髓抑制同样影响患者的生活质量,导致疲劳、生活质量降低、减少生存期等风险增加。此外,可能会导致后续治疗的疗效差,使得靶向治疗临床获益降低。肾癌靶向治疗发生的骨髓抑制,主要表现为中性粒细胞减少症。其处理原则和策略见表1。
表1 中性粒细胞减少症的处理原则

除以上针对血液学毒性管理中进行对症处理的策略外,为改善血液学不良事件的发生,应尽可能选择有效且骨髓抑制作用较小的药物。
多项临床研究的数据证实培唑帕尼血液学毒性较低。2013年发表于《新英格兰医学杂志》的COMPARZ研究是头对头对比培唑帕尼与舒尼替尼一线治疗晚期肾细胞癌的疗效与安全性的Ⅲ期临床研究。研究结果显示,培唑帕尼与舒尼替尼在肾细胞癌患者的治疗效果方面并无显著差异,但培唑帕尼的安全性和生活质量更优。经舒尼替尼治疗后,发生任何级别或3~4级白细胞减少、血小板减少、中性粒细胞减少、贫血等血液学异常患者的比例相对更高,而培唑帕尼治疗组血液学检查的波动幅度小于舒尼替尼。另一项发表于《临床肿瘤学》(JCO)杂志的PISCES研究也同样证实,培唑帕尼的各类血液学毒性反应低于舒尼替尼,且研究中大部分患者(70%)和医生(61%)均倾向于选择培唑帕尼,主要因为培唑帕尼不良反应轻,较少疲劳发生,生活质量更佳。
2、高血压
根据抗VEGF抑制剂的药物原理,其对内皮功能产生影响,抑制新小动脉和毛细血管形成并引发血管收缩。因此,治疗过程中容易出现高血压等不良反应。在培唑帕尼治疗相关高血压的临床管理中,治疗前应给予血压监测;治疗期间,应常规监测,出现高血压症状后及时给于处理。总体原则为:建议患者服用适当的降压药物,如血管转化酶抑制剂(ACEI)、血管紧张素Ⅱ受体拮抗剂(ARB)、钙通道阻滞剂(CCB),并报告相关不良反应,患者不可未经医生允许停用降压药。如出现高血压危象,或者在培唑帕尼减量且持续降压治疗时仍出现严重高血压(200/110mmHg),需停止培唑帕尼治疗。具体诊疗流程见图1-1、1-2,治疗药物剂量调整见表2。
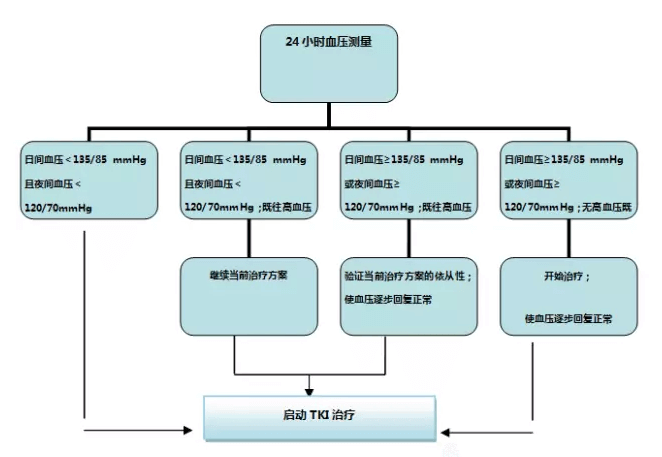
图1-1 培唑帕尼治疗相关高血压预处理的评估

图1-2 培唑帕尼治疗过程中高血压的评估和处理
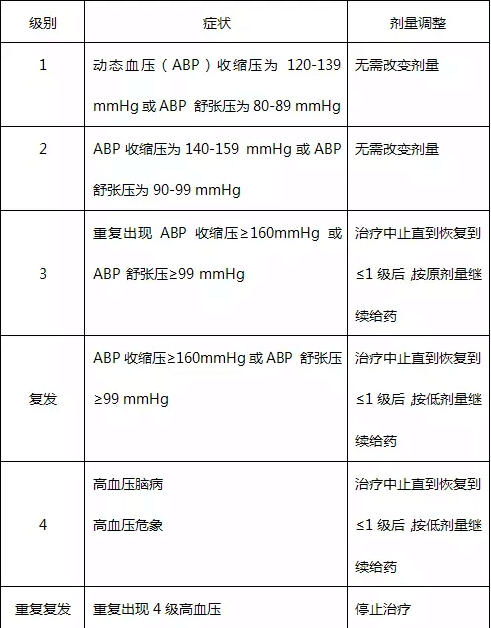
表2 TKI药物剂量调整
3、肝脏毒性
尽管培唑帕尼在患者生活质量的多个方面中显著占优,但其对肝酶水平的影响仍是医生需要关注的话题。VEG 105192研究中显示,与安慰剂组相比,培唑帕尼组最常见的实验室检查异常为谷氨酸转氨酶(ALT)增高,发生率为53%。
一项总结多瘤种共9项前瞻性II期、III期临床研究的荟萃分析中显示,纳入2080例晚期肿瘤患者,培唑帕尼治疗后发生肝脏不良事件(谷丙转氨酶ALT>3xULN)的发生率为20%,首发事件的中位时间为42天。在1830例的安全性数据库中仅发生了2例(0.1%)培唑帕尼相关的致死性肝脏事件。而87%的患者ALT水平恢复(ALT≤2.5xULN),其中30%患者未经治疗干预,就回到了0级或基线水平;另外29%患者在停药后恢复到1级或更低,然后重新使用培唑帕尼治疗,且65%患者并未反复。对首发肝脏不良时间的患者结局与预后进行分析,结果显示,绝大部分(89%)ALT升高的患者都可恢复,中位恢复时间为30天;恢复用药的患者(足量或减量)中,60%不再发生肝不良事件;前12周内无论是否发生ALT升高 >3 x ULN,患者药物肝损伤症状的发生率没有差别。
这些数据也提示我们,虽然培唑帕尼会引起肿瘤患者的肝脏不良事件,但多数不良事件能够恢复,同时在临床诊疗中,要对肝脏功能进行密切的监测,对发生的肝脏不良事件进行良好的管理,以保证患者的生活质量不受影响。主要可从以下各方面展开(具体管理流程图见图2)。①在开始治疗前、治疗的第3、5、7、9周和第3、4个月进行肝功能监测,有临床症状时也需要及时进行肝功能监测;②对患者服用的其他药物进行评估,如需要,可停用有肝毒性的药物,换用无肝毒性的等效药物;③发生肝脏不良事件后,根据指标的情况进行分类处理。在转氨酶为3~8倍ULN,不伴有胆红素升高[总胆红素(TB)<2 ULN 或直接胆红素(DB)≤35%)时,继续培唑帕尼治疗,每周监测肝功能,直至转氨酶回到1级或基线水平;在转氨酶>3倍ULN伴升高胆红素(TB>2倍ULN或DB>35%)时,应终止培唑帕尼治疗;在转氨酶>8倍ULN,不伴有胆红素升高(TB<2 ULN 或 DB ≤35%)时,应中断培唑帕尼治疗,直至转氨酶回到1级或基线水平,随后可重新使用培唑帕尼,如必要,可选择400 mg的剂量,连续8周,并每周监测肝酶水平,如转氨酶水平重新>3倍ULN,停止培唑帕尼治疗。

图2 培唑帕尼的肝脏监测和管理推荐
4、腹泻
腹泻是酪氨酸激酶抑制剂(TKI)的常见不良反应之一,根据培唑帕尼既往研究数据中对安全性的报告显示,腹泻的发生率约为54%左右,大多数腹泻为轻到中度。对于培唑帕尼所引起腹泻的治疗策略,主要参考美国临床肿瘤学会(ASCO)制定的《肿瘤治疗相关腹泻治疗指南》,其中评估腹泻情况,根据CTC不良反应分级对患者腹泻进行评估,按照1级、2级、3或4级的分级情况分别给予不同的对症治疗与处理,主要流程如下(图3),腹泻具体管理办法见表3。

图3 培唑帕尼相关腹泻的管理流程
表3 腹泻的具体管理

小 结
培唑帕尼等靶向药物不良反应的管理是晚期肾癌患者临床诊疗中不可忽视的一环。医生应加强对患者该方面内容的教育,重视药物不良反应处理,提高患者生活质量。其中包括医生要向患者解释每件不良反应事件的发生率、严重程度,是否对生命产生危险,如何预防,如何治疗等。同时,临床中医生应对各项不良事件进行密切监测,以尽快提供适当的预防和支持治疗措施,使晚期肾癌患者更大地获益。
本文仅供医学药学专业人士阅读


























 X
X