不少咚友都在密切关注着PD-1抑制剂的临床试验信息,菠菜也不例外。相信大家对招募接近尾声的PD-1抑制剂Opdivo在中国大陆地区的多中心临床试验相关信息并不陌生。
然而由于过于严格的入组标准与数量相对稀少的入组名额,大部分患者都被拦在了临床试验的大门之外,留下不少遗憾。
除了入组极为困难外,本次临床试验的试验对象仅限于非小细胞肺癌,其他癌种均未在临床试验的范围中。
不仅如此,Opdivo在中国大陆的临床试验还设置了化疗对照组与药物治疗组进行对照试验。也就意味着在入组患者中一部分不能得到PD-1抑制剂的治疗。
因此可以说Opdivo抑制剂临床试验能帮助到的患者数量其实是非常有限的。在Opdivo抑制剂中国大陆地区临床结束后,菠菜也在持续关注着关于PD-1抑制剂临床试验的消息。
可喜的是,我们伟大的祖国医疗界此刻忽然显得格外给力!
近两年,在国内PD-1市场中也出现一批“领先玩家”,包括君实生物、恒瑞医药、百济神州、嘉和生物等。
最近一段时间,国内的PD-1抑制剂也先后获批临床试验的资格,开始了国产PD-1抑制剂的患者招募。

以下列举了正在招募临床PD1实验的品牌的招募信息:
1、黑色素瘤及泌尿系统恶性肿瘤
国产重组人源化抗PD-1单克隆抗体注射液(JS001)I 期临床研究正式开始启动招募患者了!
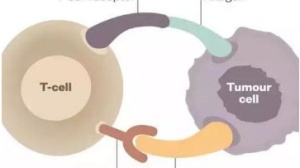
免疫治疗是近年来抗肿瘤治疗的重要方向之一,其中通过阻断PD-1/PD-L1信号通路使癌细胞死亡,具有治疗多种类型肿瘤的潜力,已经被多项国外临床研究证实可改善晚期黑色素瘤患者的总生存期。
2014年-2015年,PD-1抑制剂Nivolumab,Pembrolizumab先后于欧美及日本上市,用于治疗晚期黑色素瘤,膀胱癌及肾癌。
本研究为一项考察国产重组人源化抗PD-1单克隆抗体注射液在晚期肿瘤患者中的单次和多次给药的耐受性和药代动力学的I期、开放、单中心、剂量递增研究。拟入组黑色素瘤及泌尿系统恶性肿瘤晚期患者,约18-24例。以探索该药物在人体的安全性,并初步了解药物疗效。
如果您或您的朋友符合:
- 体力状况良好,年龄18-70岁(不限性别);
- 病理组织学或细胞学诊断黑色素瘤或泌尿系统原发的恶性肿瘤,且至少有一个器官存在转移病灶(或手术无法切除的转移病灶);
- 既往经标准治疗失败和或不能耐受标准治疗的;
- 器官功能水平良好;
- 乐于且能够遵守研究方案要求;
- 在治疗前后能够提供新鲜肿瘤组织。
那么您或您的朋友有可能符合该项研究。欢迎来北京大学肿瘤医院肾癌黑色素瘤科门诊就诊,进一步了解入组可能性。
如果您需要获得进一步的相关研究信息,您可以联系以下医生。
联系医生:唐碧霞
门诊时间:
唐碧霞(周五下午)
2、其他肿瘤

恒瑞医药抗PD-1抗体临床试验正式在中山大学肿瘤防治中心启动,即将招募实体瘤患者。

嘉和生物药业也于2016.2.22 发布最新消息:云南沃森生物技术股份有限公司(以下简称“公司”)控股子公司嘉和生物药业有限公司(以下简称“嘉和生物”)自主创新研发的抗PD-1单抗产品“杰诺单抗注射液”向上海市食品药品监督管理局提出临床研究注册申请,并于近日获得了上海市食品药品监督管理局出具的《药品注册申请受理通知书》。
产品名称:杰诺单抗注射液
剂型:注射剂
规格:7ml:70mg
申请事项:新药申请
申报阶段:临床。
注册分类:治疗用生物制品1类
申请人:嘉和生物药业有限公司
受理号:CXSL1600016沪
“杰诺单抗注射液”为嘉和生物在中国申报临床研究的第2个治疗用生物制品1类新药(之前嘉和已经有6个单抗产品申报临床研究,包括1个治疗用生物制品1类和5个治疗用生物制品2类产品)。
杰诺单抗是具有全新序列的创新抗PD-1单抗,嘉和生物拥有核心自主知识产权,其主要的潜在适应症包括各种血癌及黑色素瘤、非小细胞肺癌、肾癌等多种实体瘤。
百济神州的PD-1单抗 BGB-A317 顺利通过美国 FDA 的新药研究申请(IND)审评,并与去年6月临床一期试验已经入组了第一位患者。
五、总结
以上是截至目前已经获得临床试验审批的国产PD-1抑制剂相关招募信息,各位咚友如感兴趣的话可以尝试联系,申请入组。
但是有一点菠菜不得不郑重提醒大家:虽然目前国内多种PD-1抑制剂已经获准临床资格,且试验范围不仅限于非小细胞肺癌,临床试验中也不会有对照组的区分,也就是说,参与临床试验的患者都将得到PD-1抑制剂的治疗。
这对患者们而言无疑是非常棒的一个消息。但是由于目前开展的临床试验仅仅为一期临床试验,其实验目的在于检验国产PD-1抑制剂的安全性与剂量大小。也就是说在一期临床试验中的药物是首次用于人体,其中可能存在的安全隐患(副作用等)临床试验方也不得而知。
这就为参与临床试验的患者留下了一个安全性方面的不确定因素。虽然临床试验出现安全问题的可能性并不大,但在医疗界历史上依然是出现过一些安全事故的。
关于是否参与临床试验,还需要各位咚咚仔细斟酌考虑。菠菜仅只为大家提供这个消息,最终决定的权力还在各位手中。咚咚肿瘤科将尽全力帮助您有关于PD-1抑制剂的治疗。
也欢迎大家下载咚咚肿瘤科APP咨询肿瘤治疗各方面咨询。为您,我们还可以做的更多!
本文仅供医学药学专业人士阅读
























 X
X