过去我们往往认为放疗对远端转移没有任何作用,但随着SBRT(立体定向放疗)的出现,它能够治疗寡转移(少数的局部继发性转移,一般转移灶不超过5处),至此传统思维被打破。放疗和免疫治疗的早期实验可以追溯到2012年。
科学家们在携带三阴乳腺癌肿瘤细胞的小鼠身上做了一组实验。如下图:30只小鼠被分为6组,分别用①普通控制(左上)、②4次放疗(中上)、③5次放疗(右上)、④免疫疗法(左下)、⑤4次放疗+免疫疗法(中下)、⑥5次放疗+免疫疗法(右下)的方法进行治疗。
注:灰色为每只小鼠各自的肿瘤生长曲线,黑色为小鼠的中位肿瘤生长曲线;括号内为肿瘤完全消失的比例。

结果:可以清楚看到A图单独使用PD-1单抗或放疗对于三阴乳腺癌的小鼠模型都失败(无完全缓解)。但是PD-1与放疗的联用,加强了放疗治疗目前肿瘤以及预防继发肿瘤风险的能力。B图为小鼠接种后的第34天的肿瘤大小情况。此实验可为放疗结合免疫治疗治疗乳腺癌提供强烈依据。
放疗自20世纪初就被作为是癌症治疗的支柱之一,在最新的癌症治疗计划中,半数患者都需要接受放疗。
2014年Oncotarget刊登文章,文章指出放疗除了能杀死肿瘤细胞,还可以激活宿主的免疫系统。它改变了肿瘤微环境,从而通过增强免疫系统杀伤肿瘤。免疫药物能促进患者的抗肿瘤免疫反应。因此放疗与免疫疗法相结合理论上强强联合,会有很大的发展和应用前景。
2016年Nature Review《根治肿瘤的创新策略》文章指出,立体定向放疗可刺激免疫系统来阻止肿瘤复发和/或转移。同时,它破坏了肿瘤的支撑微环境,使得肿瘤杀伤免疫细胞更容易进入肿瘤区域;而加入外源免疫治疗后(如PD-1单抗或CTLA-4单抗),即放疗+免疫治疗,会进一步强化免疫力,降低淋巴结侵犯和远处转移,取得更高的治愈率。
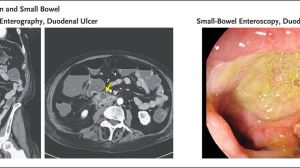
2012年一篇最早发表的相关报道,立体定向放疗(28.5 Gy/3次)与伊匹单抗连用,成功治疗转移性黑色素瘤患者的椎旁转移灶。CT扫描结果不仅证实局部效果,而且放疗野外的远处病灶也明显退缩。
2013年发表在Cancer Med的一项研究发现(39)黑色素瘤脑转移患者接受伊匹单抗治疗的同时,给予全脑放射治疗(WBRT)或立体定向放射外科(SRS)的治疗,前后的中位生存期分别为3.1个月和19.9个月。

MD Anderson肿瘤中心提供了另一则案例。该患者入组该中心的放疗+免疫治疗临床研究。
患者接受免疫治疗后,选择最大的肺转移灶给予立体定向放疗,随后继续伊匹单抗治疗。

图A为放疗前多发肺转移灶(黄色箭头),图B为放疗计划照射其中一个病灶,图C为放疗后1年的多发肺转移灶已完全消失。
目前,有多项免疫治疗+放疗的临床试验陆续展开。下图为2016年8月刊Nature Review《免疫治疗结合立体定向放疗ISABR——根治肿瘤的创新策略》中所列出的八项正在进行的临床试验。

图表可见,正在进行的临床试验大都处在I期,其中CTLA-4抗体Ipilimumab(伊匹单抗)协同或先后放疗的临床试验居多,PD-1抑制剂也开始进行联合用于肝癌和肺癌的治疗。
我们总感慨科技快速发展,可从科技出现到转化为明显的临床受益的时间却还很漫长。免疫治疗协同放疗,开启了放疗用于全身性疾病局部治疗的窗口。
探索免疫系统加强放疗效果还相对较新,但放疗不能再只被当做是局部治疗的方式,而应该是治疗实体瘤的系统性武器。
文章数据来自:
1.Ipilimumab and radiation therapy for melanoma brain metastases,2013; 2(6): 899–906,Cancer Medicine
2.Immunotherapy and stereotactic ablative radiotherapy (ISABR): a curative approach? 516 | AUGUST 2016 | VOLUME 13, Nature Review
3.Immunological interactions in radiotherapy—opening a new window of opportunity, 2016;4(3):51Ann Transl Med
4.Radiotherapy Increases the Permissiveness of Established Mammary Tumors to Rejection by Immunomodulatory Antibodies,72(13); 3163–74. 2012 AACR.
本文仅供医学药学专业人士阅读




.jpg-pd13)


.jpg-pd13)















 X
X