最近,癌症治疗领域再次传来喜讯。
北京大学肿瘤医院和南加州大学的研究团队合作,在CAR-T细胞的Ⅰ期临床试验中取得重大成果。他们精心设计和改造的新型CAR-T细胞,在合适剂量下,使72.5%的B细胞淋巴瘤患者得到缓解,其中54.5%的得到完全缓解,且疗效持久。
更重要的是,在所有接受治疗的25名患者中,没有发生一例神经毒性或严重的细胞因子释放综合征事件。而这两类副作用正是当前CAR-T细胞治疗的最大障碍。相关研究发表在顶级学术期刊《自然·医学》上,本文的通讯作者是南加州大学的陈思毅教授和北京大学肿瘤医院的朱军教授[1]。
 左:陈思毅教授(图片来自UCS) 右:朱军教授(图片来自北大肿瘤医院)
左:陈思毅教授(图片来自UCS) 右:朱军教授(图片来自北大肿瘤医院)
CAR-T细胞免疫疗法的出现,是人类癌症治疗领域的里程碑,其治疗效果之好,令人赞叹。例如,第一款获批上市的CAR-T产品Kymriah(CD19-BBz),在复发或难治性弥漫大B细胞淋巴瘤的临床试验中,使53%的患者得到客观缓解,其中40%完全缓解[2]。
随后,CAR-T又在多个临床试验中取得优异成绩,其中,一个中国团队利用CAR-T治疗多发性骨髓瘤,使100%的患者得到缓解,74%的患者达到严格完全缓解[3]。此外,这种新型的癌症治疗方法还不断向实体瘤领域扩展。
所有这些研究都表明,CAR-T细胞在癌症的治疗中具有巨大的潜力。
但是,我们也不得不承认,这些耀眼的成绩无法掩盖CAR-T治疗的重大缺陷——副作用。
CAR-T治疗最常见的副作用是细胞因子释放综合征(CRS)和神经毒性。CRS是指在免疫细胞和肿瘤细胞作用的过程中,大量释放细胞因子,这些细胞因子又会引发进一步的连锁反应,如过度炎症反应、毛细血管渗漏、凝血级联反应等,进而导致器官受损和脑肿胀,最终危及生命[4]。
 细胞因子释放综合征(图片来自creative-biolabs.com)
细胞因子释放综合征(图片来自creative-biolabs.com)
据统计,在一组接受Kymriah治疗的患者中,58%发生了CRS,其中23%为严重的3/4级。同时,还有21%的患者发生了神经毒性事件,其中12%为严重的3/4级[2]。在其他临床研究中,CAR-T治疗引起的CRS和神经毒性也并不少见。
不良事件发生比例如此之大,令人惊心,也严重阻碍了CAR-T治疗临床应用的脚步。面对这个严峻的问题,全世界的科学家也在积极寻求破解的办法,南加州大学的陈思毅教授便是其中一位。
CAR-T细胞的抗肿瘤作用,主要是其表面的嵌合抗原受体(CAR)介导的,CAR负责识别肿瘤细胞表面的抗原,进而引起特异性的抗肿瘤反应。而CRS的产生,自然也是与CAR有关的。
于是,陈思毅教授团队将重点放在了改造CAR上。他们通过蛋白结构预测软件Phrye2,仔细分析了Kymriah 的CAR(CD19-BBz)的结构,并对CD19-BBz中的CD8α片段进行改造,得到多种突变体。如下图,原版CD19-BBz的CD8α肽段含有71个氨基酸,称作CD19-BBz(71),而括号内不同的数字代表不同的CD8α肽段长度。
 CD19-BBZ(71)为原版,其他为突变体
CD19-BBZ(71)为原版,其他为突变体
随后,研究人员将这些CD19-BBz的突变体安装到T细胞上,并和肿瘤细胞作用,检测其产生细胞因子的能力。
他们发现,安装CD19-BBz(86)的CAR-T细胞与肿瘤细胞作用时,产生细胞因子的能力大幅降低,而抗肿瘤效果却并没有被削弱。随后,CD19-BBz(86) CAR-T细胞在动物实验中也展现了不俗的效果,在成功治愈大部分肿瘤小鼠的同时,并没有产生明显的CRS和神经毒性等副作用。
 CD19-BBz(86)在小鼠中治疗效果不俗,且副作用更小
CD19-BBz(86)在小鼠中治疗效果不俗,且副作用更小
在动物实验中证明其安全性和效果后,陈教授团队积极和北京大学肿瘤医院的朱军教授团队合作,开展了临床试验。
这是一项Ⅰ期临床试验(NCT02842138),在北京大学肿瘤医院进行。试验一共招募了26名难治性B细胞淋巴瘤患者,其中有25名患者接受CD19-BBz(86) CAR-T细胞治疗。另外一名因不能产生足够CAR-T细胞,而没有继续试验。
该研究一共设置了3个剂量梯度。其中,最低剂量组一共包括6名患者,他们接受注射的CD19-BBz(86) CAR-T细胞数量为3~6×106个,这些患者中,有3名患者对治疗有响应;中等剂量组包括8名患者,接受注射的CD19-BBz(86) CAR-T细胞数量为6~9×107,其中,4名患者对治疗有响应。
而最高剂量组包括11名患者,接受注射CD19-BBz(86) CAR-T细胞数量为2–4×108,共有8名患者对治疗有响应,其中6名患者肿瘤完全缓解,达到54.5%,另外2名部分缓解。检测还发现,所有这些剂量都没有超过患者的最大耐受量。
不仅如此,最高剂量组6名完全缓解的患者中的5名,在最近一次随访中,被发现CAR-T细胞的抗肿瘤效果还保持着(随访时间为153天~290天),而另外一名完全缓解患者的治疗效果也保持了162天。而在一些部分缓解的患者中,CAR-T细胞也保持了持久的抗肿瘤反应,其中一名患者在接受治疗395天后,抗肿瘤反应仍然存在。此外,研究人员还证实,这些CAR-T细胞在体内经过了增殖,并具有了对肿瘤的免疫记忆。
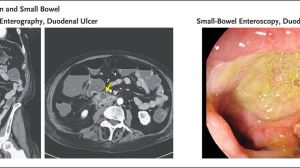
 左图为患者的CT图,右图为所有患者的治疗效果统计
左图为患者的CT图,右图为所有患者的治疗效果统计
这些数据表明,CD19-BBz(86) CAR-T细胞具有强大且持久的抗肿瘤作用。
随后,研究人员又检测了患者的副作用情况,发现了令人惊喜的结果。他们对CRS和神经毒性进行检测和评估后发现,所有25名患者中,18名没有发生CRS,而另外7名也仅仅是发生了1级CRS。而且,在所有患者中没有观察到任何神经毒性事件。严重的CRS和神经毒性事件发生率为0!
 部分患者的治疗效果统计,红框为不良事件
部分患者的治疗效果统计,红框为不良事件
这个结果令研究者们备受鼓舞。陈思毅教授说道,“改进后的CAR -T细胞在患者体内增殖并分化为记忆细胞,从而产生强大而持久的抗肿瘤效果,并且不会引起毒性。目前,毒性是CAR -T细胞治疗的最大障碍。我希望这种更安全的CAR- T细胞疗法有一天能应用于门诊病人。”[5]
他们下一步的计划是进行多中心的Ⅱ期试验,在更大的患者群体中测试安全性和有效性[5]。
本研究中所用的降低副作用的方法,在机制上还没有被完全阐明,这也是研究者们后面需要做的事。而对这个方向的探索,将为开发更好的CAR-T治疗方法奠定基础。
参考资料:
[1] Zhitao Ying et al. A safe and potent anti-CD19 CAR T cell therapy, Nature Medicine, 2019, DOI: https://doi.org/10.1038/s41591-019-0421-7
[2] Schuster S J, Svoboda J, Chong E A, et al. Chimeric antigen receptor T cells in refractory B-cell lymphomas[J]. New England Journal of Medicine, 2017, 377(26): 2545-2554.
[3] Fan F, Zhao W, Liu J, et al. Durable remissions with BCMA-specific chimeric antigen receptor (CAR)-modified T cells in patients with refractory/relapsed multiple myeloma[J]. 2017.
[4] Brudno J N, Kochenderfer J N. Chimeric antigen receptor T-cell therapies for lymphoma[J]. Nature Reviews Clinical Oncology, 2017, 15(1): 31-46.
[5]https://medicalxpress.com/news/2019-04-advance-car-t-cell-therapy-severe.html
本文仅供医学药学专业人士阅读





















 X
X