在2014年,首个PD-1抗体药物Opdivo上市以来,这类检查点抑制剂免疫疗法就像开了挂一样,三天一个小突破,五天一个大突破…
获批的适应症更是创造了肿瘤医疗史上绝无仅有的奇迹:恶性黑色素瘤、非小细胞肺癌、肾细胞癌、霍奇金淋巴瘤、头颈癌、膀胱癌、肝癌以及胃癌等多种恶性癌症。代表性药物Keytruda(pembrolizumab)更是成为了“广谱抗癌药”。
由于戴上了数不清的“突破”光环,因此很多“走投无路”的晚期癌症患者视PD-1免疫疗法为“救命稻草”。但事实上,这种免疫疗法并不是适合每一个人,临床试验表明,只有约20-40%的患者能够从中获益。

这真的是一个悲伤的消息!
先别哭
Matthew F Krummel教授表示“还有救”!

2018年6月25日,在线发表在国际著名期刊《Nature Medicine》上的一项重量级研究中,加州大学旧金山分校(UCSF)的Matthew F Krummel教授团队发现了人类癌症患者的一个关键生物学通路,而这一通路似乎可以引发免疫系统对检查点抑制剂治疗的成功应答。研究包括人类肿瘤样本的初步观察结果,小鼠模型中的机制研究以及其他患者样本的确认,可以更好地帮助临床医生预测哪些患者自然会从这些有前途的新疗法中受益,更重要的是,还可能改变另外一部分患者的免疫应答,让更多的人从这类免疫疗法中受益。


正常情况下,T细胞中的“刹车”是为了阻止它们攻击自身组织的,但癌细胞通常会通过激活T细胞中的“刹车”来逃避免疫系统的追踪。检查点抑制剂药物通过切断这些“刹车”,则可以“唤醒”免疫系统,对癌细胞发起攻击,并成功地消除了大约20 – 40 %的黑色素瘤和某些其他癌症类型患者的恶性肿瘤。
其中最好的情况是,处于亢奋状态的T细胞能够持续存在,时刻监控以防止癌症的复发。但事实并非如此,大多数患者体内的T细胞仍然处于休眠状态,任由癌细胞随意扩散,也就是我们所说的“刹车”失灵。主要免疫疗法的共同发明者之一Matthew F. Krummel教授认为,答案可能在于对占据肿瘤周围组织的更广泛的免疫细胞群体更深入的了解,例如引导T细胞找到目标的DC (树突状细胞),或者在T细胞之前担任检测和杀死癌细胞的一线战士的NK细胞(自然杀伤细胞)。
Krummel问:“如果你想让T细胞对癌症发起攻击,首先,你会不会找个帮手?
而现实情况是,我们并不知道谁是免疫系统中的好搭档和坏搭档,所以我们开始系统地切除肿瘤,并对其中的每一种细胞类型发起问话:‘你能激活T细胞吗?’”
2014年,Krummel的实验室在小鼠肿瘤中发现了一种特殊类型的树突状细胞,称为SDCs-起刺激作用的树突细胞,顾名思义,其在刺激T细胞发挥抗癌作用方面至关重要。研究人员发现,在没有SDC的小鼠肿瘤中,T细胞不能有效地对检查点抑制剂免疫疗法产生应答,而且,具有低SDC水平的肿瘤患者的临床治疗结果也相对较差。
所以问题来了,为什么只有部分肿瘤中会存在这类保护性的SDCs?
NK细胞提高免疫治疗应答率和癌症生存率
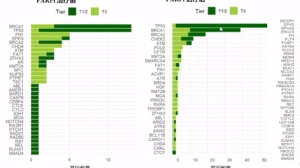
在今天这项最新的研究中,Kevin Barry为共同负责人,Krummel的团队首次使用来自癌症基因组图谱(TCGA)中公开的黑色素瘤基因组学数据和来自UCSF临床合作者的组织样本证明:人黑色素瘤中SDCs的数量能够预测患者的免疫治疗应答和总生存期,正如之前在小鼠中观察到的结果一样。

BDCA-3 + DCs定义了黑色素瘤患者的总体预后并预测对抗PD-1免疫疗法的反应(图片来源 nature)
为了解释为什么有些患者的SDC比其他患者多,研究人员将肿瘤样本分解成它们的组成细胞,旨在发现其与SDC数量较多的肿瘤中基因表达的差异。结果,研究人员发现,被称为FLT3LG的特异性免疫信号蛋白或细胞因子的表达与SDCs的存在紧密相关。
在进一步的研究中,研究人员发现FLT3LG由另一类称为自然杀伤细胞(NK)的免疫细胞表达。另外,小鼠实验表明,NK细胞能够直接控制肿瘤中SDCs存在的数量。
对此,Krummel说:“最有趣的发现之一是,我们早就知道自然杀伤细胞可以直接杀死癌细胞。但在这项新研究中,我们发现NK细胞并不只是简单粗暴的杀死癌细胞,它还具有和其他免疫细胞交流的能力。我们可以很直接看到NK细胞非常离散和选择性地向SDCs传递细胞因子。”
根据以上发现,研究人员得出了一个假设:激活的NK细胞在患者肿瘤中能够募集SDCs,使患者对免疫治疗产生更强烈的应答。

NK细胞和BDCA-3+ DC水平以及黑素瘤患者的抗PD-1反应具有独特的相关性(图片来源 nature)
在验证研究中,该团队分析了临床合作者提供的人肿瘤样品中存在的NK细胞,结果发现:肿瘤中NK细胞的存在与SDCs数量的增加以及患者对PD-1抗体药物的长期反应和总体存活率相关。
换句话说,如果研究人员能够找到一种增加患者肿瘤中NK细胞的方法,那么就可以提高肿瘤内SDCs的数量,进而对目前的检查点抑制剂免疫疗法产生更强烈的应答。显然,这是非常令人兴奋的,因为已经有一些基于NK细胞开发的新型免疫疗法正在开展临床试验。
另外,这项新发现的另一个潜在应用是:NK细胞和SDCs水平可以作为生物标记物,以预测患者能否对免疫疗法产生应答。
但目前,研究人员只能依赖于依赖活检或手术切除的肿瘤样本对其进行检测,但如果可以在血液中找到相关检测因子,那么对临床上确定免疫治疗有效的患者具有很大的意义。
最后,需要提及的是,这项研究的实现离不开临床合作者的大力支持,作为UCSF免疫组织联合会的一部分,他们提供了研究中分析的关键黑色素瘤组织样本。其中该联合会是由Krummel与制药巨头艾伯维(AbbVie)、安进(Amgen)以及百时美施贵宝(BMS)合作创立的一项积极而长远的计划,旨在分析来自10多种不同癌症的数百个肿瘤样本的免疫学特征。

What we do(图片来源 immunoprofiler.org)
未来,Krummel希望进一步扩大这一项目,不仅仅是了解对某些治疗反应良好或较差的肿瘤在免疫细胞群体方面的差异性,还包括在健康和患病的状态下,对整个身体的免疫系统的完整动态范围进行分析
Krummel 说:“这是免疫系统的模式,它并不只是随机分类的独立细胞。揭示与积极治疗相关的免疫细胞关系是很令人兴奋的,因为它告诉了我们健康的免疫群体是什么样的,也就是说,我们离揭开健康和疾病的根本原因又近了一步。简言之,每次转弯都让我们离迷宫的中心更近。”
参考出处:
https://www.ucsf.edu/news/2018/06/410911/immune-profile-successful-cancer-immunotherapy-discovered
https://www.nature.com/articles/s41591-018-0085-8
http://immunoprofiler.org/
doi: 10.1016/j.ccell.2014.09.007
本文来源:医麦客
本文仅供医学药学专业人士阅读





.jpg-pd13)
















 X
X